[رقم سجل المستخلصات الكيميائية 5402-55-1] 2-ثيوفينيثانول
معيار المنتج
| مظهر | Clorless إلى سائل شفاف أصفر فاتح |
| اختبار الهوية | يتوافق وقت الاستبقاء مع مرجع GC |
| نقاء | 99٪ min. (GC)) |
| 3-ثيوبنين الإيثانول | 0.1٪ كحد أقصى (GC) |
| النجاسة الفردية (مجهول) | 0.2٪ كحد أقصى (GC) |
| محتوى الماء | 0.3٪ كحد أقصى (W / W) |
| فترة إعادة الاختبار | سنة واحدة |
تفاصيل المنتج [5402-55-1]
| CAS رقم. : | 5402-55-1 | رقم MDL: | MFCD00005462 |
| معادلة : | C6H8OS | نقطة الغليان : | 223 درجة مئوية عند 760 مم زئبق |
| صيغة الهيكل الخطي: | - | مفتاح InChI: | غير متاح |
| ميغاواط: | 128.19ز / مول | معرف Pubchem: | 79400 |
| المرادفات: | |||
كيمياء محسوبة لـ [5402-55-1]
الخصائص الفيزيائية والكيميائية
| رقم.ذرات ثقيلة: | 8 |
| رقم.اروم.ذرات ثقيلة: | 5 |
| كسر Csp3: | 0.33 |
| رقم.روابط قابلة للدوران: | 2 |
| رقم.متقبلات السندات H: | 1.0 |
| رقم.المانحون H- بوند: | 1.0 |
| الانكسار المولي: | 35.25 |
| TPSA: | 48.47Ų |
الدوائية
| امتصاص الجهاز الهضمي: | عالي |
| تأثير BBB: | نعم |
| الركيزة P-gp: | No |
| مثبط CYP1A2: | No |
| مثبط CYP2C19: | No |
| مثبط CYP2C9: | No |
| مثبط CYP2D6: | No |
| مثبط CYP3A4: | No |
| سجل Kp (نفاذ الجلد): | -6.18 سم / ثانية |
شحوم
| سجل Po / w (iLOGP): | 1.75 |
| سجل Po / w (XLOGP3): | 1.27 |
| سجل Po / w (WLOGP): | 1.28 |
| سجل Po / w (MLOGP): | 0.84 |
| سجل Po / w (SILICOS-IT): | 2.67 |
| إجماع سجل Po / w: | 1.56 |
المخدرات
| ليبينسكي: | 0.0 |
| شبح: | لا أحد |
| فيبر: | 0.0 |
| إيغان: | 0.0 |
| Muegge: | 1.0 |
| نقاط التوافر البيولوجي: | 0.55 |
الذوبان في الماء
| سجل S (ESOL): | -1.77 |
| الذوبان: | 2.2 مجم / مل ؛0.0172 مول / لتر |
| فصل : | قابل للذوبان جدا |
| سجل S (علي): | -1.89 |
| الذوبان: | 1.66 مجم / مل ؛0.013 مول / لتر |
| فصل : | قابل للذوبان جدا |
| السجل S (SILICOS-IT): | -1.86 |
| الذوبان: | 1.77 مجم / مل ؛0.0138 مول / لتر |
| فصل : | قابل للذوبان |
الكيمياء الطبية
| الآلام: | 0.0 تنبيه |
| برينك: | 0.0 تنبيه |
| الرصاص: | 1.0 |
| إمكانية الوصول الاصطناعية: | 1.82 |
أمان [5402-55-1]
| كلمة الإشارة: | تحذير | فصل: | غير متاح |
| البيانات التحذيرية: | P261-P305 + P351 + P338 | الأمم المتحدة#: | غير متاح |
| بيانات الأخطار: | H302-H315-H319-H335 | مجموعة التعبئة: | غير متاح |
| الرسم التخطيطي GHS: |  | ||
البيانات التحذيرية - عام
| شفرة | عبارة |
| ص 101 | إذا كانت هناك حاجة إلى مشورة طبية ، فاحرص على وجود حاوية أو ملصق المنتج في متناول اليد. |
| ص 102 | يحفظ بعيدا عن متناول الأطفال. |
| ص 103 | اقرأ الملصق قبل الاستخدام |
وقاية
| شفرة | عبارة |
| ص 201 | الحصول على تعليمات خاصة قبل الاستخدام. |
| ص 202 | لا تتعامل معه حتى تتم قراءة وفهم جميع احتياطات السلامة. |
| P210 | الابتعاد عن الحرارة / الشرر / اللهب المكشوف / الأسطح الساخنة.- ممنوع التدخين. |
| P211 | لا ترش على اللهب المكشوف أو أي مصدر اشتعال آخر. |
| P220 | يحفظ / يخزن بعيدًا عن الملابس / المواد القابلة للاشتعال. |
| ص 221 | اتخذ أي احتياطات لتجنب الاختلاط مع المواد القابلة للاحتراق |
| ص222 | لا تسمح بالتلامس مع الهواء. |
| ص223 | الابتعاد عن أي اتصال محتمل مع الماء ، بسبب رد الفعل العنيف واحتمال حدوث وميض. |
| P230 | حافظ على الرطوبة |
| P231 | التعامل مع الغاز الخامل. |
| P232 | يحفظ بعيداً عن الرطوبة. |
| P233 | إبقاء الحاويات مغلقة بإحكام. |
| P234 | تبقي فقط في الحاوية الأصلية. |
| P235 | اهدء |
| P240 | تأريض / ربط الحاوية ومعدات الاستقبال. |
| ص 241 | استخدم معدات كهربائية / تهوية / إضاءة / معدات مقاومة للانفجار. |
| P242 | استخدم فقط الأدوات التي لا تسبب شرارة. |
| P243 | اتخاذ تدابير وقائية ضد التفريغ ثابت. |
| P244 | حافظ على صمامات الاختزال خالية من الشحوم والزيوت. |
| P250 | لا تخضع للطحن / الصدمة / الاحتكاك. |
| ص 251 | حاوية مضغوطة: لا تخترقها أو تحرقها حتى بعد الاستخدام. |
| P260 | لا تستنشق الغبار / الدخان / الغاز / الضباب / الأبخرة / الرذاذ. |
| ص 261 | تجنب استنشاق الغبار / الدخان / الغاز / الضباب / الأبخرة / الرذاذ. |
| ص 262 | لا تدخل في العين أو الجلد أو الملابس. |
| ص 263 | تجنب الاتصال أثناء الحمل / أثناء الرضاعة. |
| ص 264 | اغسل يديك جيدا بعد الانتهاء. |
| ص 265 | اغسل الجلد جيدًا بعد التعامل معه. |
| P270 | لا تأكل أو تشرب أو تدخن عند استخدام هذا المنتج. |
| ص 271 | استخدم فقط في الهواء الطلق أو في منطقة جيدة التهوية. |
| ص 272 | لا ينبغي السماح لملابس العمل الملوثة بالخروج من مكان العمل. |
| ص 273 | تجنب إطلاق للبيئة. |
| P280 | قم بارتداء القفازات الواقية / الملابس الواقية / واقي العين / واقي الوجه. |
| ص 281 | استخدام معدات الوقاية الشخصية على النحو المطلوب. |
| ص 282 | قم بارتداء القفازات العازلة الباردة / واقي الوجه / واقي العين. |
| ص 283 | ارتدِ ملابس مقاومة للحريق / اللهب. |
| P284 | ارتداء حماية الجهاز التنفسي. |
| ص 285 | في حالة عدم كفاية التهوية ، قم بارتداء واقي للجهاز التنفسي. |
| P231 + P232 | التعامل مع الغاز الخامل.يحفظ بعيداً عن الرطوبة. |
| P235 + P410 | اهدء.يحفظ بعيداً عن أشعة الشمس. |
إجابة
| شفرة | عبارة |
| P301 | أذا تم أبتلاعها: |
| P304 | في حالة الاستنشاق: |
| P305 | إذا كان في العين: |
| P306 | في حالة ارتداء الملابس: |
| P307 | إذا تعرضت: |
| P308 | في حالة التعرض أو القلق: |
| P309 | إذا تعرضت أو شعرت بتوعك: |
| P310 | اتصل على الفور بمركز السموم أو الطبيب / الطبيب. |
| P311 | اتصل بمركز السموم أو الطبيب / الطبيب. |
| P312 | اتصل بمركز السموم أو الطبيب / الطبيب إذا شعرت بتوعك. |
| P313 | احصل على استشارة / رعاية طبية. |
| P314 | احصل على استشارة / رعاية طبية إذا شعرت بتوعك. |
| P315 | احصل على استشارة / رعاية طبية فورية. |
| P320 | |
| P302 + P352 | في حالة السقوط على الجلد: اغسله بالكثير من الصابون والماء. |
| ص 321 | |
| ص 322 | |
| P330 | اشطف الفم. |
| P331 | لا تقم بتحريض القيء. |
| P332 | في حالة حدوث تهيج في الجلد: |
| P333 | في حالة حدوث تهيج أو طفح جلدي: |
| P334 | يغمر في ماء بارد / لف ضمادات مبللة. |
| P335 | تخلص من الجزيئات السائبة من الجلد. |
| P336 | قم بإذابة الأجزاء المجمدة بالماء الفاتر.لا تفرك المنطقة المصابة. |
| P337 | في حالة استمرار تهيج العين: |
| P338 | إزالة العدسات اللاصقة، إذا كانت موجودة وسهلة للقيام.استمر في الشطف. |
| P340 | انقل الضحية إلى الهواء النقي واحتفظ بالراحة في وضع مريح للتنفس. |
| ص 341 | إذا كان التنفس صعبًا ، انقل المصاب إلى الهواء النقي وحافظ على الراحة في وضع مريح للتنفس. |
| ص 342 | إذا كنت تعاني من أعراض تنفسية: |
| P350 | اغسلها برفق بالكثير من الصابون والماء. |
| ص 351 | شطف بحذر بالماء لعدة دقائق. |
| ص 352 | اغسلها بكمية كبيرة من الصابون والماء. |
| ص 353 | اشطف الجلد بالماء / الاستحمام. |
| P360 | اشطف الملابس والجلد الملوث على الفور بكمية كبيرة من الماء قبل خلع الملابس. |
| ص 361 | قم بإزالة / خلع جميع الملابس الملوثة على الفور. |
| ص 362 | خلع الملابس الملوثة وتغسل قبل إعادة استخدامها. |
| ص 363 | اغسل الملابس الملوثة قبل إعادة الاستخدام. |
| P370 | في حالة نشوب حريق: |
| ص 371 | في حالة نشوب حريق كبير وبكميات كبيرة: |
| ص 372 | خطر الانفجار في حالة نشوب حريق. |
| ص 373 | لا تكافح النار عندما تصل النار إلى متفجرات. |
| P374 | كافح النيران باحتياطات عادية من مسافة معقولة. |
| ص 376 | وقف تسرب إذا آمن للقيام بذلك.الغازات المؤكسدة (القسم 2.4) 1 |
| ص 377 | تسرب غاز حريق: لا تطفئ إلا إذا كان من الممكن إيقاف التسرب بأمان. |
| P378 | |
| P380 | منطقة الإخلاء. |
| ص 381 | تخلص من جميع مصادر الاشتعال إذا كان ذلك آمنًا. |
| P390 | امتصاص الانسكاب لمنع تلف المواد. |
| ص 391 | جمع الانسكاب.خطرة على البيئة المائية |
| P301 + P310 | في حالة الابتلاع: اتصل على الفور بمركز السموم أو الطبيب / الطبيب. |
| P301 + P312 | في حالة الابتلاع: اتصل بمركز السموم أو الطبيب / الطبيب إذا شعرت بتوعك. |
| P301 + P330 + P331 | في حالة الابتلاع: اشطف الفم.لا تقم بتحريض القيء. |
| P302 + P334 | في حالة السقوط على الجلد: اغمره في ماء بارد / لفه بضمادات مبللة. |
| P302 + P350 | في حالة السقوط على الجلد: اغسله برفق بكمية كبيرة من الصابون والماء. |
| P303 + P361 + P353 | في حالة السقوط على الجلد (أو الشعر): انزع / اخلع جميع الملابس الملوثة على الفور.اشطف الجلد بالماء / الدش. |
| P304 + P312 | في حالة الاستنشاق: اتصل بمركز السموم أو الطبيب / الطبيب إذا شعرت بتوعك. |
| P304 + P340 | في حالة الاستنشاق: انقل المصاب إلى الهواء النقي واحتفظ بالراحة في وضع مريح للتنفس. |
| P304 + P341 | في حالة الاستنشاق: إذا كان التنفس صعبًا ، انقل المصاب إلى الهواء النقي واحتفظ بالراحة في وضع مريح للتنفس. |
| P305 + P351 + P338 | في حالة دخول العينين: اشطفها بالماء بحذر لعدة دقائق.إزالة العدسات اللاصقة، إذا كانت موجودة وسهلة للقيام.استمر في الشطف. |
| P306 + P360 | في حالة ارتداء الملابس: اشطف الملابس والجلد الملوث على الفور بكمية كبيرة من الماء قبل نزع الملابس. |
| P307 + P311 | في حالة التعرض للسموم: اتصل بمركز السموم أو الطبيب / الطبيب. |
| P308 + P313 | في حالة التعرض أو القلق: احصل على استشارة / رعاية طبية. |
| P309 + P311 | إذا تعرضت أو شعرت بتوعك: اتصل بمركز السموم أو الطبيب / الطبيب. |
| P332 + P313 | في حالة حدوث تهيج للبشرة: احصل على استشارة / رعاية طبية. |
| P333 + P313 | في حالة حدوث تهيج أو طفح جلدي: احصل على استشارة / رعاية طبية. |
| P335 + P334 | تخلص من الجزيئات السائبة من الجلد.اغمرها في ماء بارد / لفها بضمادات مبللة. |
| P337 + P313 | إذا استمر تهيج العين: احصل على استشارة / رعاية طبية. |
| P342 + P311 | إذا كنت تعاني من أعراض تنفسية: اتصل بمركز السموم أو الطبيب / الطبيب. |
| P370 + P376 | في حالة نشوب حريق: أوقف التسريب إذا كان ذلك آمناً. |
| P370 + P378 | في حالة نشوب حريق: |
| P370 + P380 | في حالة نشوب حريق: اخلاء المنطقة. |
| P370 + P380 + P375 | في حالة نشوب حريق: اخلاء المنطقة.مكافحة النيران عن بعد بسبب خطر الانفجار. |
| P371 + P380 + P375 | في حالة نشوب حريق كبير وبكميات كبيرة: اخلاء المنطقة.مكافحة النيران عن بعد بسبب خطر الانفجار. |
تخزين
| شفرة | عبارة |
| ص 401 | |
| ص 402 | تخزينها في مكان جاف. |
| P403 | يخزن في مكان جيد التهوية. |
| P404 | تخزينها في وعاء مغلق. |
| P405 | مخزن مغلق. |
| ص 406 | تخزينها في حاوية مقاومة للتآكل مع بطانة داخلية مقاومة. |
| ص 407 | الحفاظ على فجوة هوائية بين الأكوام / المنصات. |
| P410 | يحفظ بعيداً عن أشعة الشمس. |
| P411 | |
| P412 | لا تعرض لدرجات حرارة تتجاوز 50 درجة مئوية / 122 درجة فهرنهايت. |
| P413 | |
| P420 | تخزين بعيدا عن المواد الأخرى. |
| P422 | |
| P402 + P404 | تخزينها في مكان جاف.تخزينها في وعاء مغلق. |
| P403 + P233 | يخزن في مكان جيد التهوية.إبقاء الحاويات مغلقة بإحكام. |
| P403 + P235 | يخزن في مكان جيد التهوية.اهدء. |
| P410 + P403 | يحفظ بعيداً عن أشعة الشمس.يخزن في مكان جيد التهوية. |
| P410 + P412 | يحفظ بعيداً عن أشعة الشمس.لا تعرض لدرجات حرارة تتجاوز 50 درجة مئوية / 122 درجة فهرنهايت. |
| P411 + P235 | اهدء. |
تصرف
| شفرة | عبارة |
| ص 501 | تخلص من المحتويات / الحاوية في ... |
| ص 502 | الرجوع إلى الصانع / المورد للحصول على معلومات حول الاستعادة / إعادة التدوير |
الأخطار المادية
| شفرة | عبارة |
| H200 | متفجرات غير مستقرة |
| H201 | مادة متفجرة؛خطر الانفجار الشامل |
| H202 | مادة متفجرة؛خطر الإسقاط الشديد |
| H203 | مادة متفجرة؛خطر نشوب حريق أو انفجار أو بروز |
| H204 | خطر الحريق أو الإسقاط |
| H205 | قد تنفجر جماعي في النار |
| H220 | غاز لهوب للغاية |
| H221 | غاز قابل للاشتعال |
| H222 | الهباء الجوي سريع الاشتعال |
| H223 | الهباء الجوي القابل للاشتعال |
| H224 | سائل وبخار لهوب للغاية |
| H225 | سائل وبخار شديد الاشتعال |
| H226 | سائل وبخار قابل للاشتعال |
| H227 | سائل قابل للاشتعال |
| H228 | مادة صلبة قابلة للاشتعال |
| H229 | حاوية مضغوطة: قد تنفجر إذا تم تسخينها |
| H230 | قد تتفاعل بشكل متفجر حتى في حالة عدم وجود هواء |
| H231 | قد تتفاعل بشكل متفجر حتى في حالة عدم وجود هواء عند ضغط و / أو درجة حرارة مرتفعة |
| H240 | قد يتسبب التسخين في حدوث انفجار |
| H241 | قد يتسبب التسخين في نشوب حريق أو حدوث انفجار |
| H242 | قد يؤدي التسخين إلى نشوب حريق |
| H250 | تلتقط النار بشكل تلقائي إذا تعرضت للهواء |
| H251 | التسخين الذاتيقد تشتعل فيها النيران |
| H252 | التسخين الذاتي بكميات كبيرة ؛قد تشتعل فيها النيران |
| H260 | عند التلامس مع الماء ، تطلق غازات قابلة للاشتعال قد تشتعل تلقائيًا |
| H261 | عند التلامس مع الماء تطلق غازات قابلة للاشتعال |
| H270 | قد يتسبب في نشوب حريق أو يزيد من حدته ؛مؤكسد |
| H271 | قد يتسبب في نشوب حريق أو انفجار ؛مؤكسد قوي |
| H272 | قد تزيد من حدة النار.مؤكسد |
| H280 | يحتوي على غاز تحت الضغطقد تنفجر إذا تم تسخينها |
| H281 | يحتوي على غاز مبردقد يسبب حروقًا أو إصابات شديدة البرودة |
| H290 | قد تكون أكالة للمعادن |
المخاطر الصحية
| شفرة | عبارة |
| H300 | مميت إذا ابتلع |
| H301 | سام إذا ابتلع |
| H302 | ضارة إذا ابتلعت |
| H303 | قد تكون ضارة إذا ما ابتلع |
| H304 | قد تكون قاتلة إذا ابتلع ودخل المسالك الهوائية |
| H305 | قد يكون ضارًا إذا ابتلع ودخل الشعب الهوائية |
| H310 | مميت إذا تلامس مع الجلد |
| H311 | سام عند ملامسته للجلد |
| H312 | ضار عند ملامسته للجلد |
| H313 | قد تكون ضارة عند ملامستها للجلد |
| H314 | يسبب حروقا جلدية شديدة وتلفا للعين |
| H315 | يسبب تهيج الجلد |
| H316 | يسبب تهيج الجلد الخفيف |
| H317 | قد يسبب رد فعل حساسية الجلد |
| H318 | يسبب ضررًا خطيرًا للعين |
| H319 | يسبب تهيج العين خطيرة |
| H320 | يسبب تهيج العين |
| H330 | مميت إذا استنشق |
| H331 | سام إذا استنشق |
| H332 | ضار إذا استنشق |
| H333 | قد يكون ضارًا إذا تم استنشاقه |
| H334 | قد يسبب أعراض الحساسية أو الربو أو صعوبات في التنفس إذا تم استنشاقه |
| H335 | قد يسبب تهيجا في الجهاز التنفسي |
| H336 | قد تسبب النعاس أو الدوار |
| H340 | قد تسبب عيوبًا وراثية |
| H341 | يشتبه في تسببه في عيوب وراثية |
| H350 | قد يسبب السرطان |
| H351 | يشتبه في تسببه في الإصابة بالسرطان |
| H360 | قد يضر بالخصوبة أو الجنين |
| H361 | يشتبه في إضراره بالخصوبة أو الجنين |
| H361d | يشتبه في إلحاق الضرر بالجنين |
| H362 | قد يسبب ضررًا للأطفال الذين يرضعون رضاعة طبيعية |
| H370 | يسبب تلف الأعضاء |
| H371 | قد يتسبب في تلف الأعضاء |
| H372 | يسبب تلف الأعضاء من خلال التعرض المطول أو المتكرر |
| H373 | قد يتسبب في تلف الأعضاء من خلال التعرض المطول أو المتكرر |
خطر بيئي
| شفرة | عبارة |
| H400 | شديدة السمية للحياة المائية |
| H401 | سامة للحياة المائية |
| H402 | ضار بالحياة المائية |
| H410 | شديدة السمية للحياة المائية مع تأثيرات طويلة الأمد |
| H411 | سامة للحياة المائية مع تأثيرات طويلة الأمد |
| H412 | ضار بالحياة المائية وله تأثيرات طويلة الأمد |
| H413 | قد يسبب آثارًا ضارة طويلة الأمد للحياة المائية |
| H420 | يضر بالصحة العامة والبيئة من خلال تدمير طبقة الأوزون في الغلاف الجوي العلوي |
التطبيق في توليف [5402-55-1]
مسار توليف المنبع من [5402-55-1]
طريق اصطناعي في المصب [5402-55-1]
مسار توليف المنبع من [5402-55-1]
| أَثْمَر | شروط رد الفعل | العملية في التجربة |
|---|---|---|
| 72٪ | مع سلالة من الفطريات zygomycete S..Racemosum MUT 770 في ثنائي ميثيل سلفوكسيد لمدة 72 ساعة ؛تفاعل إنزيمي | 2.3تجارب التحول الأحيائي تم زرع السلالات الفطرية مسبقًا في أطباق بتري التي تحتوي على وسط صلب مالتستكست (MEA: 20 جم لتر جلوكوز ، 20 جم لتر مستخلص الشعير ، 20 جم لتر أجار ، 2 جم لتر ببتون) من اللقاح. للثقافات السائلة.تم تلقيح الفطر على شكل كونيديا معلق (1110 كونيديا / مل) في 50 مل تطلب 40 مل من وسط سائل مالتستكست.تم تحضين القوارير عند 25 درجة مئوية وتم الحفاظ عليها تحت التحريض (110 دورة في الدقيقة). بعد يومين من النمو الأولي ، تمت إضافة محلول 500 ملي مولار من الركيزة DMSO ، إلى تركيز ركيزة ابتدائي (c0) من 1-5 ملي مولار.لكل ركيزة ، تم إجراء ثلاث مكررات بيولوجية. تم إجراء التجربة لمدة 3 أيام بعد إضافة الطبقات الفرعية ، وخلال هذه الفترة تم أخذ عينات 1 مل ، في فترات زمنية محددة (عادة 24 و 48 و 72 ساعة).تم استخلاص كل عينة باستخدام EtOAc (500 لتر) ، وتم تجفيف الطور العضوي فوق اللامائى Na2SO4 وتحليلها باستخدام GC / MS.في بعض الحالات (انظر القسم 2.4) تم عزل المنتج المختزل ، ولكل مجموعة من التحولات الحيوية ، تم استخدام طلب واحد للتأكد من الكتلة الحيوية الأولية ودرجة الحموضة قبل إضافة الركيزة. تم التقييم في نهاية التجربة لجميع الأسئلة.تم فصل الوسائط السائلة عن ترشيح الكتلة الحيوية واستخدمت لقياس الأس الهيدروجيني بينما تم تجفيف الفطريات عند 60 درجة مئوية لمدة 24 ساعة لقياس الوزن الجاف للكتلة الحيوية.2- (ثيوفين -2 يل) إيثانول: من 2- (ثيوفين -2-يل) حامض أسيتيك (3.7 مجم ، 72 فى المائة) ومن ميثيل 2- (ثيوفين -2-يل) أسيتات (24.6 مجم ، 96 فى المائة).1H NMR (400 ميجا هرتز ، CDCl3 ، TMS): = 7.20 (م ، 1H ، هيدروجين غير متجانس ماتيك) ، 6.99 (م ، 1H ، هيدروجين غير متجانس) ، 6.90 (م ، 1 ساعة ، هيدروجين غير متجانس) ، 3.85 (طن ، 2 ساعة ، J = 6.2 هرتز ، CH2OH) ، 3.02 (طن ، 2H ، J = 6.2 هرتز ، CH2CH2OH).13C NMR (100 ميجا هرتز ، CDCl3 ، TMS): = 140.5 ، 127.0 ، 125.8 ، 124.0 ، 63.4 ، 33.3.GC / MS: tR = 9.47 دقيقة ، m / z128 (M + ، 30) ، 110 (5) ، 97 (100) |
| 66.5٪ | المرحلة رقم 1: مع رباعي هيدريد الليثيوم والألومنيوم في رباعي هيدرو الفوران عند 0-20 درجة مئوية ؛ المرحلة الثانية: بالماء ؛كلوريد الصوديوم في رباعي هيدرو الفوران عند 0 ؛ | الخطوة 9 2- (Thiophen-2-yl) الإيثانول: عند حوالي 0 درجة مئوية ، تمت إضافة محلول من حمض أسيتيك ثيوفين -2-يل (1.0 جم ؛ 7.03 ملي مول) في رباعي هيدروفيوران (10 مل) بالتنقيط إلى معلق من هيدريد ألومنيوم الليثيوم (0.534 جم ، 14.05 ملي مول) في جاف. تتراهيدروفوران (10 مل). تم تقليب الخليط عند درجة حرارة محيطة لمدة 4 ساعات ، ثم تم تبريده إلى حوالي 0 درجة مئوية. بعد إضافة محلول كلوريد صوديوم مشبع بارد (1 مل) ، يرشح الخليط ، وتغسل الأملاح غير العضوية باستخدام رباعي هيدرو فوران وأسيتات إيثيل. تم الجمع بين ناتج الترشيح والغسالات وتركيزهما في وسط مفرغ لإعطاء مركب العنوان كزيت بني (0.600 جم ؛ 66.5 في المائة). 1H NMR (400 ميجا هرتز ، CDCl3) δ 1.60 (ر ، قابلة للاستبدال بـ د2O ، 1H) ، 3.08 (t ، J = 6.2 هرتز ، 2H) ، 3.85 (t ، J = 6.2 هرتز ، 2H) ، 6.87-6.88 (م ، 1H) ، 6.95-6.97 (م ، 1H) ، 7.16-7.25 (م ، ح 1).الأشعة تحت الحمراء (فيلم) υ 3345 ، 3105 ، 2211 ، 2126 ، 2090 ، 1792 ، 1433 ، 1138 ، 972 ، 737 ، 699 سم-1MS: 129 (ذكور + 1). |
| أَثْمَر | شروط رد الفعل | العملية في التجربة |
|---|---|---|
| 96٪ | مع سلالة من الفطريات zygomycete S..Racemosum MUT 770 في ثنائي ميثيل سلفوكسيد لمدة 72 ساعة ؛تفاعل إنزيمي | 2.3تجارب التحول الأحيائي تم زرع السلالات الفطرية مسبقًا في أطباق بتري التي تحتوي على وسط صلب مالتستكست (MEA: 20 جم لتر جلوكوز ، 20 جم لتر مستخلص الشعير ، 20 جم لتر أجار ، 2 جم لتر ببتون) من اللقاح. للثقافات السائلة.تم تلقيح الفطر على شكل كونيديا معلق (1110 كونيديا / مل) في 50 مل تطلب 40 مل من وسط سائل مالتستكست.تم تحضين القوارير عند 25 درجة مئوية وتم الحفاظ عليها تحت التحريض (110 دورة في الدقيقة). بعد يومين من النمو الأولي ، تمت إضافة محلول 500 ملي مولار من الركيزة DMSO ، إلى تركيز ركيزة ابتدائي (c0) من 1-5 ملي مولار.لكل ركيزة ، تم إجراء ثلاث مكررات بيولوجية. تم إجراء التجربة لمدة 3 أيام بعد إضافة الطبقات الفرعية ، وخلال هذه الفترة تم أخذ عينات 1 مل ، في فترات زمنية محددة (عادة 24 و 48 و 72 ساعة).تم استخلاص كل عينة باستخدام EtOAc (500 لتر) ، وتم تجفيف الطور العضوي فوق اللامائى Na2SO4 وتحليلها باستخدام GC / MS.في بعض الحالات (انظر القسم 2.4) تم عزل المنتج المختزل ، ولكل مجموعة من التحولات الحيوية ، تم استخدام طلب واحد للتأكد من الكتلة الحيوية الأولية ودرجة الحموضة قبل إضافة الركيزة. تم التقييم في نهاية التجربة لجميع الأسئلة.تم فصل الوسائط السائلة عن ترشيح الكتلة الحيوية واستخدمت لقياس الأس الهيدروجيني بينما تم تجفيف الفطريات عند 60 درجة مئوية لمدة 24 ساعة لقياس الوزن الجاف للكتلة الحيوية.2- (ثيوفين -2 يل) إيثانول: من 2- (ثيوفين -2-يل) حامض أسيتيك (3.7 مجم ، 72 فى المائة) ومن ميثيل 2- (ثيوفين -2-يل) أسيتات (24.6 مجم ، 96 فى المائة).1H NMR (400 ميجا هرتز ، CDCl3 ، TMS): = 7.20 (م ، 1H ، هيدروجين غير متجانس ماتيك) ، 6.99 (م ، 1H ، هيدروجين غير متجانس) ، 6.90 (م ، 1 ساعة ، هيدروجين غير متجانس) ، 3.85 (طن ، 2 ساعة ، J = 6.2 هرتز ، CH2OH) ، 3.02 (طن ، 2H ، J = 6.2 هرتز ، CH2CH2OH).13C NMR (100 ميجا هرتز ، CDCl3 ، TMS): = 140.5 ، 127.0 ، 125.8 ، 124.0 ، 63.4 ، 33.3.GC / MS: tR = 9.47 دقيقة ، m / z128 (M + ، 30) ، 110 (5) ، 97 (100) |
طريق اصطناعي في المصب [5402-55-1]
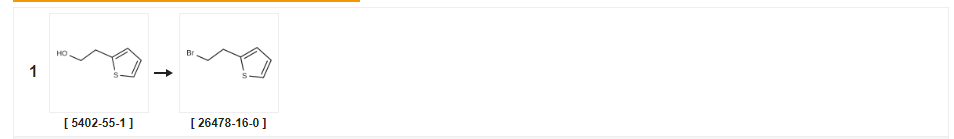
| أَثْمَر | شروط رد الفعل | العملية في التجربة |
|---|---|---|
| 94٪ | مع رباعي بروميد الكربون ؛ثلاثي فينيل فوسفين في رباعي هيدرو الفوران عند 0 ؛تقنية شلينكجو خامل؛ | |
| 69٪ | مع البرومثلاثي فينيل فوسفين في ثنائي كلورو ميثان عند 20 درجة مئوية ؛ | |
| 64٪ | ص 31 تخليق 2- (2-برومو إيثيل) ثيوفين مثال الإنتاج 31 تمت معالجة تخليق 2- (2-برومو إيثيل) ثيوفين 2- ثينيل إيثانول (0.44 مل) كما في مثال الإنتاج 1 أعلاه لإعطاء مركب العنوان (0.490 جم) كزيت عديم اللون (العائد: 64.0٪).1H-NMR (400 ميجا هرتز ، CDCl3): δ (جزء في المليون) 3.38 (2H ، t ، J = 7.6 هرتز) ، 3.58 (2H ، t ، J = 7.6 هرتز) ، 6.89 (1H ، d ، J = 1.2 هرتز) ، 6.96 (1H ، d ، J = 4.2Hz) ، 7.19 (1H ، dd ، J = 1.2 ، 4.2Hz). |
| 28٪ | مع ثلاثي بروميد الفوسفور في ثنائي كلورو ميثان عند 0 - 20 ؛لمدة 1 ساعة | |
| 19٪ | مع ثلاثي بروميد الفوسفور في رباعي كلورو ميثان عند 65 درجة مئوية ؛لـ 0.333333 ساعة ؛ | a تمت إضافة ثلاثي بروميد الفوسفور (2.0 مل ، 21.1 ملي مول) إلى محلول مقلب من 2- (ثيوفين -2-يل) إيثانول (2.25 جم ، 17.6 ملي مول) في رابع كلوريد الكربون (162 مل) ثم يسخن الخليط عند 65 درجة مئوية لـ. 20 دقيقة.تم ترك الخليط ليبرد إلى درجة الحرارة المحيطة ثم يضاف الثلج.تم فصل الطبقة العضوية ثم الطبقة المائية المستخرجة باستخدام ثنائي كلورو ميثان (2 × 30 مل).تم غسل الطبقات العضوية المجمعة بمحلول ملحي ، ثم تجفيف (NaSO4) ، وترشيحها وتقليلها في وسط مفرغ.تمت تنقية المتبقي بواسطة كروماتوجرافيا الوميض فوق السيليكا ، تمت التصفية التتابعية باستخدام أسيتات إيثيل: مخاليط الهكسان 0: 100 إلى 0.5: 95.5 لإعطاء 2- (2-برومو إيثيل) ثيوفين كزيت بني (650 مجم ، 19٪). |
| مع بيريدينالكلوروفورم.الفوسفور ثلاثي البروميد | ||
| مع ثلاثي بروميد الفوسفور في ثنائي إيثيل إيثر عند 0 ؛لمدة 4 ساعات | مثال ثنائي الأبعاد ثنائي الأبعاد ؛9- (4،5-Dimethyl-thiazol-2-yl) -4- [4- (2-thiophen-2-yl-ethyl) -piperazin-1-yl] -5،6،7، 8- TETRAHYDRO- 1 ، 3 ، 4B-TRIAZA-FLUORENE إلى محلول من 2- (2-ثينيل) إيثانول (1.63 جم) في إيثر جاف (15 مل) عند 0 درجة مئوية تمت إضافة PBr3 (1. 31 مل) بالتنقيط.بعد 4 ساعات يخفف خليط التفاعل مع داي كلورو ميثان ، ويغسل بالماء ، ويجفف (MGS04) ويزال المذيب في وسط مفرغ للحصول على زيت بني ينقى باستخدام كروماتوجراف فلاش لينتج 2- (2-برومو-إيثيل) -ثيوفين.خليط من 9- (4، 5-DIMETHYL-THIAZOL-2-YL) -4-PIPERAZIN-1-YL-5، 6،7، 8-TETRAHYDRO- 1، 3، 4b-triaza-fluorene (85mg) ، تم تسخين 2- (2-برومو-إيثيل) -ثيوفين (44 مجم) وكربونات البوتاسيوم (38 مجم) لإعادة تكثيف البخار في أسيتونيتريل (5 مل) لمدة 4 ساعات.تم تبريد خليط التفاعل ، واستخلاصه إلى ثنائي كلورو ميثان ، وتجفيفه (MGS04) وإزالة المذيب في وسط مفرغ للحصول على منتج خام تم تنقيته باستخدام كروماتوجرافيا فلاش للحصول على مركب العنوان (30 مجم). |
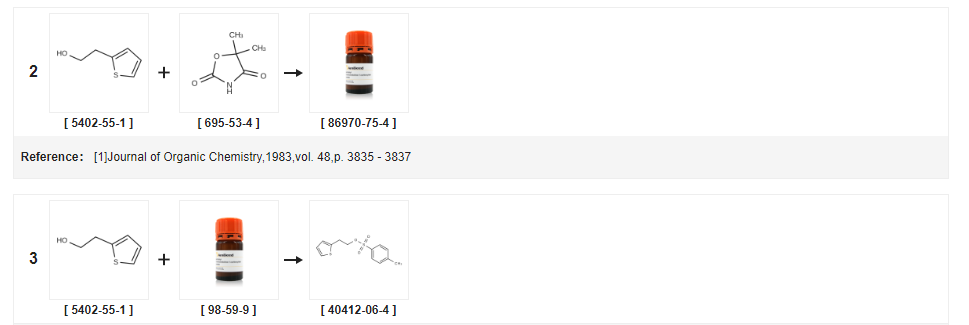
| أَثْمَر | شروط رد الفعل | العملية في التجربة |
|---|---|---|
| 98٪ | مع ثلاثي إيثيل أمينعند 35 درجة مئوية ؛ تبريد بالثلج ؛ | تمت إضافة (0.87 مول) من 2-ثيوفينيثانول و 184 جم (0.97 مول) من p-toluenesulfonyl chloride بالتتابع إلى دورق ثلاثي العنق سعة 1 لتر ، تمت إضافة 98 جم (0.97 مول) من ثلاثي إيثيل أمين بالتنقيط إليها تحت حمام ماء مثلج ، والحفاظ على درجة حرارة سائل التفاعل لا تزيد عن 20 درجة مئوية ، والإسقاط النهائي ، والتسخين إلى 35 درجة مئوية لمواصلة التحريك ، على التوالي 24 ساعة ، وأخذ العينات 27 ساعة ، TLC ، حتى يكتمل التفاعل ، وقف التفاعل ، والترشيح ، وكعكة الترشيح بالمناسبة تم تجفيف كمية من ثنائي كلورو ميثان وطبقة كلوريد الميثيلين بكبريتات الصوديوم اللامائية لمدة ساعتين.تم ترشيح المادة المجففة وغسل المادة المجففة بكمية صغيرة من كلوريد الميثيلين.يتم فك ضغط ناتج الترشيح في وسط مفرغ وتبخر المادة المرشحة تحت ضغط منخفض.يتركز لوزن ثابت ليكون زيت بني يزن 203 جرام ينتج 98٪ |
| 96.37٪ | مع ثلاثي إيثيل أمينفي التولوينفي 5 - 30 ℃ ؛لمدة 20.8333 ساعة ؛ توزيع / انتقائية المنتج ؛ | مثال 3 تحضير 2-Thienylethyl Para-Toluenesulphonate (الصيغة السابعة) باستخدام تولوين 400 لتر من التولوين و 163.2 كجم من بارا-تولوين سلفونيل كلوريد تم شحنه في مفاعل نظيف وجاف متبوعًا بالتبريد إلى حوالي 5 م. 100 كجم من ثيوفين- تمت إضافة 2-إيثانول عند حوالي 5 درجة مئوية خلال حوالي 20 دقيقة متبوعًا بإضافة 130 كجم من ثلاثي إيثيل أمين خلال حوالي 8 ساعات و 50 دقيقة.تم رفع درجة حرارة خليط التفاعل إلى حوالي 30 درجة مئوية متبوعًا بالتقليب لمدة 12 ساعة تقريبًا.ترشح كتلة التفاعل من خلال مرشح Nutsche وتغسل بـ 2 * 100 لتر من التولوين.ينقل ناتج التفاعل إلى مفاعل آخر يليه الغسل بـ 5 * 200 لتر من الماء.تم فصل الطبقات العضوية والمائية وتم تقطير الطبقة العضوية تمامًا عند أقل من 70 درجة مئوية تحت ضغط منخفض للحصول على 212 كجم (العائد: 96.37٪) من مركب العنوان.نقاء GC: 95.59٪. |
| 96.5٪ | مع ثلاثي إيثيل أمينفي ثنائي كلورو ميثانفي -5 - 20 ℃ ؛لمدة 2 ساعة | 32.7 جم (0.17 مول) من p-toluenesulfonyl chloride ، 40 مل من ثنائي كلورو ميثان في دورق التفاعل ، تبرد إلى -5 درجة مئوية ، 20 جم (0.16 مول) 2-ثيوفينيثانول تمت إضافة 28.4 جم (0.28 مول) من ثلاثي إيثيل أمين ببطء بالتنقيط و تم الحفاظ على درجة حرارة محلول التفاعل عند حوالي 0 درجة مئوية بالإضافة إلى Bi ، وتم تحضينه لمدة ساعتين بعد تدفئة التفاعل إلى درجة حرارة الغرفة.2-ثيوفين إيثانول ليتم استهلاكه حتى المواد الخام ، الترشيح بالشفط ، تغسل المادة الصلبة بكمية صغيرة من كلوريد الميثيلين وتغسل المادة المرشحة بـ 50 مل من بيكربونات الصوديوم المشبعة وتجفف فوق كبريتات الصوديوم اللامائية.الترشيح ، تركيز المادة المرشحة ، مادة صلبة بنية فاتحة مترسبة ، مفلترة ، مغسولة بكمية قليلة من إيثر البترول إلى الأبيض ، أي P-toluenesulfonate-2-thiophene ethyl ester 42.5 g ، ينتج 96.5٪ (نقاء HPLC 99٪) |
| 95.5٪ | مع ثلاثي إيثيل أمينفي ثنائي كلورو ميثانعند 7.5 - 22.5 ℃ ؛لمدة 5 ساعات ؛ توزيع / انتقائية المنتج ؛ | مثال 10 تحضير 2- (2-ثيوفين) Ethanol Tosylate (الصيغة VII) باستخدام ثنائي كلورو ميثان تمت إضافة 4 لترات من ثنائي كلورو ميثان إلى مفاعل عند درجة حرارة حوالي 30 درجة مئوية ، وتم تبريده إلى درجة حرارة حوالي 7.5 درجة مئوية. تمت إضافة 1.784 كجم من p-toluene sulphonyl chloride متبوعًا بـ 1 كجم من thiophene-2-ethanol.تمت إضافة 1.302 كجم من ثلاثي إيثيل أمين إلى كتلة التفاعل المذكورة أعلاه عند درجة حرارة حوالي 7.5 درجة مئوية متبوعًا برفع درجة حرارة كتلة التفاعل ببطء إلى 22.5 درجة مئوية لمدة 5 ساعات تقريبًا.تم ترشيح كتلة التفاعل التي تم الحصول عليها من خلال مرشح ضغط Nutsche ، وغسلها باستخدام كلوريد ميثيلين (2 * 1 لتر) وتم جمع المحلول الأم ونقله إلى مفاعل آخر.تم غسل الطبقة العضوية بالماء (5 * 2 لتر).تم تعريض الطبقة العضوية التي تم الحصول عليها بهذه الطريقة للتقطير عند درجة حرارة أقل من 70 درجة مئوية باستخدام دوران الماء الساخن.تم بعد ذلك تبريد المادة المتبقية التي تم الحصول عليها إلى حوالي 30 درجة مئوية للحصول على 2.1 كجم (ينتج: 95.5٪) من مركب العنوان. |
| 93.6٪ | مع ثلاثي إيثيل أمينفي التولوينعند 45 ؛لمدة 4 ساعات | مثال 1 0.2.تحويل (S) -1 ، 2،3،4-رباعي هيدرو-5-هفدروكسي- N- بروبيل- النفثالين-2-هيدروبروميد الأمونيوم (VIII) إلى ملح هيدروكلوريد للروتيجوتين ؛10.2.1.تحضير 2- (2-ثينيل) إيثيل -4-تولوين سلفونات ؛يتم الجمع بين 4-تولوين سلفونيل كلوريد (162 جم) ، والتولوين (363.3 جم) و2- (2-ثينيل) إيثانول (104 جم).يضاف ثلاثي إيثيل أمين (93 جم) للحفاظ على درجة حرارة أقل من 45 درجة مئوية. بعد 4 ساعات ، يغسل الخليط بحمض الفوسفوريك المائي ، هيدروكسيد الصوديوم المائي ثم الماء.يتم تقطير الطور العضوي في الفراغ.يضاف الأيزوبروبانول (314 جم) و هيبتانات (365.9 جم).تتم بلورة الدفعة عن طريق التبريد وعزلها عند -15 درجة مئوية ، ويتم ترشيح البلورات وغسلها باستخدام هيبتانات (175 مل).ثم يتم تجفيف البلورات تحت فراغ عند درجة حرارة الغرفة حتى يتم الحصول على نقطة انصهار أكبر من 30 درجة مئوية. الناتج (214 جم): تحليل HPLC 93.6٪ نقاوة مؤكدة> 99٪ و 100٪ مقارنة بالمعيار المرجعي. |
| 93.6٪ | مع ثلاثي إيثيل أمينفي التولوينعند 45 ؛لمدة 4 ساعات | يتم الجمع بين 4-تولوين سلفونيل كلوريد (162 جم) ، والتولوين (363.3 جم) و2- (2-ثينيل) إيثانول (104 جم).يضاف ثلاثي إيثيل أمين (93 جم) للحفاظ على درجة حرارة أقل من 45 درجة مئوية. بعد 4 ساعات ، يغسل الخليط بحمض الفوسفوريك المائي ، هيدروكسيد الصوديوم المائي ثم الماء.يتم تقطير الطور العضوي في الفراغ.يضاف الأيزوبروبانول (314 جم) و هيبتانات (365.9 جم).تتم بلورة الدفعة عن طريق التبريد وعزلها عند -15 درجة مئوية ، ويتم ترشيح البلورات وغسلها باستخدام هيبتانات (175 مل).يتم بعد ذلك تجفيف البلورات تحت ضغط مفرغ عند درجة حرارة الغرفة حتى يتم الحصول على نقطة انصهار تبلغ 30 درجة مئوية.[0255] العائد (214 جم): 93.6٪ |
| 90٪ | مع هلام السيليكافي ثنائي كلورو ميثانلمدة ساعتين | 12.8 جم (0.1 مول) 2- (2- ثينيل) إيثانول ، 1000 مل من ثنائي كلورو ميثان ، 21.0 جم (0.12 مول) من كلوريد حمض p-toluenesulfonic و 10.0 جم من هلام السيليكا في دورق التفاعل ، تمت إعادة تدفق التفاعل لمدة ساعتين ، يبرد ، يرشح لإزالة هلام السيليكا. يغسل خليط التفاعل تباعاً بالماء المقطر ، محلول كربونات الصوديوم المشبع ، محلول ملحي ، ثم يُزال مذيب كلوريد الميثيلين بالتقطير تحت ضغط مخفض ، لإعطاء 26.0 جم من p- تولوين سلفونيك أسيد. تحضير 2 - (2-ثينيل) إيثيل استر ، عائد 90٪. |
| في بيريدينماء؛ | (أ) تمت إضافة 2- (2-هيدروكسي إيثيل) ثيوفين توسيلات تولوين -4-سلفونيل كلوريد (4.125 جم) جزئيًا على مدار 5 دقائق إلى محلول مثلج بارد من 2- (2-هيدروكسي إيثيل) ثيوفين (1.723 جم) في بيريدين لا مائي (20 مل) ويقلب المحلول الأصفر الباهت الناتج عند صفر درجة مئوية. بعد 3 ساعات يصب خليط التفاعل في ماء مقلب بقوة (160 مل) منتجا راسب.بعد التبريد ، تم جمع المادة الصلبة وغسلها بالماء لإعطاء بلورات بيضاء من العنوان tosylate (3.555 جم) ، mp 33-34 C. ، lambdamax (EtOH) 227 نانومتر (E11612). | |
| مع ثلاثي إيثيل أمينفي البيوتانونعند 0-30 ℃ ؛ | مثال 1 تحضير 2- (2-ثينيل) -إيثيل بارا-تولوين سلفونات. يبرد إلى 0 درجة مئوية.تبع ذلك إضافة قطرة الحكيمة لثلاثي إيثيل أمين (283.1 مل) عند 0-5 درجة مئوية خلال فترة من ساعة إلى ساعتين ، وتم تقليب كتلة التفاعل لمدة 12 إلى 15 ساعة عند 25-3 درجة مئوية.تم ترشيح الكتلة الناتجة وغسلها باستخدام ميثيل إيثيل كيتون (500 مل).تم غسل الطبقة العضوية الناتجة باستخدام ماء (500 مل) متبوعًا بغسل بمحلول مشبع من بيكربونات الصوديوم (500 مل) ومحلول ملحي (500 مل).تم تقطير الطبقة العضوية الناتجة تحت ضغط أقل من 50 درجة مئوية لإعطاء 2- (2- ثينيل) -إيثيل بارا-تولوين سلفونات ككتلة زيتية (وزن الزيت: 505 جم ؛ نقاء بواسطة HPLC: 97٪). | |
| مع ثلاثي إيثيل أمينفي البيوتانونعند 0-30 ℃ ؛ | مثال 1 تحضير 2- (2-ثينيل) -إيثيل بارا-تولوين سلفونات. تم تبريده إلى صفر درجة مئوية ، تبع ذلك إضافة قطرة حكيمة لثلاثي إيثيل أمين (283.1 مل) عند 0-5 درجة مئوية خلال فترة من ساعة إلى ساعتين ، وتم تقليب كتلة التفاعل لمدة 12 إلى 15 ساعة عند 25-30 درجة مئوية. تم ترشيح الكتلة الناتجة وغسلها باستخدام ميثيل إيثيل كيتون (500 مل).تم غسل الطبقة العضوية الناتجة باستخدام ماء (500 مل) متبوعًا بغسل بمحلول مشبع من بيكربونات الصوديوم (500 مل) ومحلول ملحي (500 مل).تم تقطير الطبقة العضوية الناتجة تحت ضغط أقل من 50 درجة مئوية لإعطاء 2- (2-ثينيل) -إيثيل بارا-تولوين سلفونات ككتلة زيتية (وزن الزيت: 505 جم ؛ نقاء بواسطة HPLC: 97٪). | |
| مع كربونات البوتاسيومفي التولوينعند 0-20 ℃ ؛لمدة 3.5 ساعة ؛ | تمت إضافة 500 مل من التولوين إلى دورق تفاعل سعة 1000 مل ، و 50 جم من إيثانول الثيوفين ، و 80 جم من كلوريد ف - تولوين سلفونيل كلوريد ، وتشغيل التحريك ، تمت إضافة درجة حرارة مضبوطة بالتنقيط عند 0 كربون 64 جم من كربونات البوتاسيوم ، واستمرت الإضافة لمدة 30 دقيقة تقريبًا ، بالتنقيط يتم التسخين النهائي إلى 20 درجة مئوية من التفاعل لمدة 3 ساعات ، إلى محلول التفاعل يضاف 400 مل من الماء ، ويغسل مرتين ، ويتم استخدام طبقة التولوين المغسولة مباشرة للتفاعل التالي. | |
| مع N-ethyl-N ، N-diisopropylamine ؛في التولوينعند 0-20 ℃ ؛لمدة 3.5 ساعة ؛ | تمت إضافة 500 مل من التولوين إلى دورق تفاعل سعة 1000 مل ، و 50 جم من إيثانول ثيوفين و 92 جم من كلوريد ف - تولوين سلفونيل ، تم التقليب عند 0 درجة مئوية ، 62 جم من N ، تم إسقاط N-diisopropylethylamine لمدة 30 دقيقة تقريبًا.عند اكتمال الإسقاط ، يسخن الخليط إلى 20 درجة مئوية ويتفاعل لمدة 3 ساعات.إلى محلول التفاعل يضاف 400 مل من الماء ، ويغسل مرتين ، ويتم استخدام طبقة التولوين المغسولة مباشرة للتفاعل التالي. | |
| مع ثلاثي إيثيل أمينفي التولوينعند 0-20 ℃ ؛لمدة 3 ساعات | تم وضع 500 مل من التولوين ، و 50 جم من ثيوفين الإيثانول و 80 جم من p-toluenesulfonyl chloride في دورق تفاعل 1000 مل ، وتم رفع درجة الحرارة إلى 20 درجة مئوية لمدة 3 ساعات.يضاف 400 مل من الماء إلى محلول التفاعل ، ويغسل مرتين ، ويغسل بالتولوين ، ويضاف مباشرة إلى الخطوة التالية من التفاعل. | |
| مع كربونات البوتاسيومفي التولوينعند 0-20 ℃ ؛لمدة 3.5 ساعة ؛ | تم وضع 500 مل من التولوين ، و 50 جم من إيثانول ثيوفين ، و 107 جم من ف - تولوين سلفونيل كلوريد في دورق تفاعل سعة 1000 مل ، وتم تشغيل التقليب ، وتم التحكم في درجة الحرارة عند 0 درجة مئوية ، وإضافة 64 جم كربونات البوتاسيوم بالتنقيط ، واستمرت الإضافة حوالي 30 دقيقة ، وبعد ذلك يتم تدفئته إلى 20 درجة مئوية وتفاعله لمدة 3 ساعات ، يضاف إلى محلول التفاعل 400 مل من الماء ، ويغسل مرتين ، ويتم استخدام طبقة التولوين المغسولة مباشرة للتفاعل التالي. | |
| مع ثلاثي إيثيل أمينفي التولوينعند 0-25 ℃ ؛لمدة 3.5 ساعة ؛ | مثال 1 تتضمن طريقة تحضير هيدروكلوريد تيكلوبيدين كما هو موضح في الشكل 2 الخطوات التالية: 1.حماية p-toluenesulfonyl: في دورق تفاعل سعة 1000 مل ، تم شحن 500 مل من التولوين ، و 50 جم من إيثانول ثيوفين و 80 جم من p-toluenesulfonyl chloride ، وتم تقليبها للتحكم في درجة حرارة 0 مئوية ، تمت إضافة 47 جم من ثلاثي إيثيل أمين بالتنقيط ، تنقيط لمدة 30 دقيقة ، وترفع درجة الحرارة إلى 25 درجة مئوية لمدة 3 ساعات. يضاف 400 مل من الماء ، ويغسل مرتين ، ويغسل بطبقة تولوين مباشرة إلى الخطوة التالية من التفاعل.تفاعل التكثيف تمت إضافة محلول تفاعل التولوين في الخطوة السابقة إلى دورق تفاعل سعة 1000 مل ، متبوعًا بإضافة 114 جم من o- كلورو بنزيل أمين والتسخين إلى 90 درجة مئوية لمدة 3 ساعات.بعد التفاعل ، يبرد الخليط إلى 25 Cمئوية ويقلب لمدة ساعة.تمت إضافة ناتج الترشيح مع 200 مل من الماء ، وحمض الهيدروكلوريك ، اضبط الرقم الهيدروجيني للنظام إلى 8.5 ، وقم بتقسيم الطبقة العليا من التولوين إلى طبقات واستمر في إسقاط حمض الهيدروكلوريك لضبط الرقم الهيدروجيني إلى 5 ، ثم تبريد النظام إلى 2 جتم خلط البلورات من أجل 4 ساعات وترشيحها ، وتجفف عجينة المرشح في وسط مفرغ عند 50 ْم لإعطاء 96 جم من هيدروكلوريد التكثيف.حلقة تفاعل مغلقة إلى دورق التفاعل سعة 1000 مل يضاف 96 جم من هيدروكلوريد التكثيف ، 400 مل من 1.3-ديوكسان و 5 مل من حمض الهيدروكلوريك ، إلى 90 درجة مئوية لمدة 6 ساعات.بعد التفاعل ، يبرد الخليط إلى 7 Cمئوية ويقلب لمدة 3 ساعات.تم غسل عجينة المرشح بكمية صغيرة من 1،3-ديوكسيتان بعد 50 درجة مئوية من التجفيف بالتفريغ ، يتم الحصول على 95 جم من هيدروكلوريد تيكلوبيدين 4؟مكرر في دورق تفاعل سعة 1000 مل ، تمت إضافة 95 جم من هيدروكلوريد التيكلوبيدين الخام و 500 مل من الإيثانول المطلق وتسخينه إلى 72 درجة مئوية مع التحريك ، بعد حوالي 10 دقائق من إذابة المادة الصلبة تمامًا عن طريق إضافة 2 جم كربون نشط ، وتبييض العزل بعد 20 دقيقة من التحريك. مرشح ساخن ، يبرد المرشح تدريجيًا تتبلور البلورات عند 4 درجات مئوية لمدة 4 ساعات وترشح.تم غسل عجينة المرشح بكمية صغيرة من الإيثانول المطلق وتجفيفها في وسط مفرغ عند 50 درجة مئوية لإعطاء 91 جم من نواتج tithiol hydrochloride الدقة.إجمالي العائد 82٪ ، نقاء 99.9٪ | |
| مع هيدروكسيد الصوديومفي الماء؛التولوين.في 10 - 55 ؛لمدة 11 ساعة | في دورق ثلاثي العنق ، تم وضع 97 جم من p-toluenesulfonyl chloride و 180 مل من التولوين. يتم التقليب والإذابة ، والترشيح ، والحفاظ على الدفء عند 15-20 درجة مئوية ، و 60 جم من 2-ثيوفينيثانول و 60 مل من التولوين. دورق ثلاثي العنق ، 120 جم 40٪ هيدروكسيد صوديوم مائي ، مع التقليب ، يضاف محلول من 97 جم من p- تولوين سلفونيل كلوريد مذاب في 180 مل من التولوين بالتنقيط عند 10-20 درجة مئوية ، ويقلب الخليط لمدة 3 ساعات ، ثم يسخن إلى 45-55 درجة مئوية لمدة 8 ساعات ، ويسمح له بالوقوف في حالة التقسيم الطبقي. يتم إزالة الضغط من المرحلة العضوية لإزالة التولوين لإعطاء 2- (2-ثيوفين) إيثانول p-toluenesulfonate. زيت بني أحمر ؛الصيغة الجزيئية كما يلي: | |
| 235.1 جرام | مع هيدروكسيد الصوديومفي الكلوروفورمفي 0-5 ℃ ؛لمدة 12 ساعة | إلى دورق التفاعل ، الخطوة 2 - ثيوفين إيثانول أعلاه: 112 جم ، كلوروفورم 600 جم ، PTSC 249.4 جم ، وتم تبريد الخليط إلى 0-5 درجة مئوية ، إضافة 834 جم بنسبة 10٪ بواسطة محلول هيدروكسيد الصوديوم الكتلي ، والتحكم في درجة الحرارة 0 -5 درجة مئوية ، احتفظ بالدفء لمدة 12 ساعة ، أضف حمض الهيدروكلوريك إلى درجة الحموضة = 12 ، طبقة ، يتم استخلاص طبقة الماء مع 300 جم من الكلوروفورم ، ويتم دمج طبقة الكلوروفورم.بعد الغسل بـ 100 جم من الماء ، تم تقطير الطبقة العضوية حتى التجفيف لإعطاء 2-ثيوفينيثانول p-toluenesulfonate: 235.1 جم ينتج 95.3٪ ، نقاء 99.5٪. |
اكتب رسالتك هنا وأرسلها إلينا

![[رقم سجل المستخلصات الكيميائية 5402-55-1] 2-ثيوفينيثانول صورة مميزة](https://www.ohlsenwin.com/uploads/p1.png)
![[رقم سجل المستخلصات الكيميائية 5402-55-1] 2-ثيوفينيثانول](https://www.ohlsenwin.com/uploads/p1-300x300.png)
![[رقم سجل المستخلصات الكيميائية 5402-55-1] 2-ثيوفينيثانول](https://www.ohlsenwin.com/uploads/product-2-300x300.png)
![[رقم سجل المستخلصات الكيميائية 5402-55-1] 2-ثيوفينيثانول](https://www.ohlsenwin.com/uploads/product-1-300x300.png)





![[CAS No. 141109-14-0] (S) -Methyl 2-amino-2- (2-chlorophenyl) acetate](https://www.ohlsenwin.com/uploads/Chlorophenylglycine-methyl-ester-2-300x300.png)
![[رقم سجل المستخلصات الكيميائية 141109-19-5] (S) - ميثيل 2- (2-كلوروفينيل) -2 - ((2- (ثيوفين-2-يل) إيثيل) أمينو) أسيتات هيدروكلوريد](https://www.ohlsenwin.com/uploads/Chlorophenylglycine-methyl-ester-31-300x300.png)
![[CAS No. 40412-06-4] 2- (Thiophen-2-yl) ethyl 4-methylbenzenesulfonate](https://www.ohlsenwin.com/uploads/ethanol-Tosylate-4-300x300.png)