[CAS № 5402-55-1] 2-тиофенэтанол
стандарт продукта
| Появление | Прозрачная жидкость от бесцветного до светло-желтого цвета |
| Проверка личности | Время удерживания соответствует эталону GC |
| Чистота | 99% мин. (ГХ)) |
| 3-тиопненовый этанол | 0,1% макс. (ГХ) |
| Индивидуальная примесь (неизвестный) | 0,2% макс. (ГХ) |
| Содержание воды | 0,3% макс. (Вт/Вт) |
| Период повторного тестирования | Один год |
Подробная информация о продукте [ 5402-55-1 ]
| Номер КАС: | 5402-55-1 | № лей: | MFCD00005462 |
| Формула: | C6H8OS | Точка кипения : | 223°С при 760 мм рт.ст. |
| Формула линейной структуры: | - | Ключ ИнЧИ: | Н/Д |
| МВт: | 128,19г/моль | Идентификатор публикации: | 79400 |
| Синонимы : | |||
Расчетный химический состав [ 5402-55-1 ]
Физико-химические свойства
| номертяжелые атомы: | 8 |
| номераромат.тяжелые атомы: | 5 |
| Фракция Csp3: | 0,33 |
| номервращающиеся связи: | 2 |
| номерАкцепторы Н-связи: | 1,0 |
| номерДоноры Н-связи: | 1,0 |
| Молярная рефракция: | 35,25 |
| TPSA: | 48,47Ų |
Фармакокинетика
| Всасывание в ЖКТ: | Высокий |
| Постоянная BBB: | Да |
| Субстрат P-gp: | No |
| Ингибитор CYP1A2: | No |
| Ингибитор CYP2C19: | No |
| Ингибитор CYP2C9: | No |
| Ингибитор CYP2D6: | No |
| Ингибитор CYP3A4: | No |
| Log Kp (кожное проникновение): | -6,18 см/с |
Липофильность
| Журнал Po/w (iLOGP): | 1,75 |
| Журнал Po/w (XLOGP3): | 1,27 |
| Журнал Po/w (WLOGP): | 1,28 |
| Журнал Po/w (MLOGP): | 0,84 |
| Журнал Po/w (SILICOS-IT): | 2,67 |
| Журнал консенсуса Po/w: | 1,56 |
Сходство с наркотиками
| Липински: | 0,0 |
| Гоша: | Никто |
| Вебер: | 0,0 |
| Иган: | 0,0 |
| Мюгге: | 1,0 |
| Оценка биодоступности: | 0,55 |
Растворимость воды
| Лог S (ESOL): | -1,77 |
| Растворимость: | 2,2 мг/мл;0,0172 моль/л |
| Сорт : | Очень растворимый |
| Лог С (Али): | -1,89 |
| Растворимость: | 1,66 мг/мл;0,013 моль/л |
| Сорт : | Очень растворимый |
| Журнал S (SILICOS-IT): | -1,86 |
| Растворимость: | 1,77 мг/мл;0,0138 моль/л |
| Сорт : | Растворимый |
Медицинская химия
| БОЛИ: | 0.0 оповещение |
| Бренк: | 0.0 оповещение |
| Свинцовое сходство: | 1,0 |
| Синтетическая доступность: | 1,82 |
Безопасность [ 5402-55-1 ]
| Сигнальное слово: | Предупреждение | Сорт: | Н/Д |
| Заявления о мерах предосторожности: | П261-П305+П351+П338 | ООН#: | Н/Д |
| Заявления об опасности: | Х302-Х315-Х319-Х335 | Группа упаковки: | Н/Д |
| Пиктограмма СГС: |  | ||
Общие положения о мерах предосторожности
| Код | Фраза |
| P101 | Если необходима медицинская консультация, имейте под рукой контейнер с продуктом или этикетку. |
| Р102 | Храните в недоступном для детей месте. |
| P103 | Прочтите этикетку перед использованием |
Профилактика
| Код | Фраза |
| P201 | Получите специальные инструкции перед использованием. |
| P202 | Не работайте, пока не прочитаете и не поймете все меры предосторожности. |
| P210 | Хранить вдали от тепла/искр/открытого огня/горячих поверхностей.- Курение запрещено. |
| P211 | Не распылять на открытое пламя или другие источники воспламенения. |
| P220 | Хранить/хранить вдали от одежды/горючих материалов. |
| P221 | Примите все меры предосторожности, чтобы избежать смешивания с горючими веществами. |
| P222 | Не допускать контакта с воздухом. |
| P223 | Беречь от любого возможного контакта с водой из-за бурной реакции и возможного возгорания. |
| P230 | Держите смоченным |
| P231 | Работайте в среде инертного газа. |
| P232 | Беречь от влаги. |
| P233 | Держите контейнер плотно закрытым. |
| P234 | Хранить только в оригинальной упаковке. |
| P235 | Сохранять хладнокровие |
| P240 | Заземлить/склеить контейнер и приемное оборудование. |
| P241 | Использовать взрывозащищенное электрическое/вентиляционное/осветительное/оборудование. |
| P242 | Используйте только искробезопасный инструмент. |
| P243 | Примите меры предосторожности против статического разряда. |
| P244 | Не допускайте попадания смазки и масла на редукционные клапаны. |
| P250 | Не подвергать шлифованию/ударам/трению. |
| P251 | Контейнер под давлением: не прокалывать и не сжигать даже после использования. |
| P260 | Не вдыхать пыль/дым/газ/туман/пары/аэрозоль. |
| P261 | Избегайте вдыхания пыли/дыма/газа/тумана/паров/аэрозоля. |
| P262 | Не допускать попадания в глаза, на кожу или одежду. |
| P263 | Избегайте контакта во время беременности/во время кормления грудью. |
| P264 | Тщательно вымойте руки после обработки. |
| P265 | Тщательно вымойте кожу после обработки. |
| P270 | Не ешьте, не пейте и не курите при использовании этого продукта. |
| P271 | Используйте только на открытом воздухе или в хорошо проветриваемом помещении. |
| P272 | Загрязненную рабочую одежду нельзя выносить за пределы рабочего места. |
| P273 | Избегайте попадания в окружающую среду. |
| P280 | Носите защитные перчатки/защитную одежду/защиту глаз/защиту лица. |
| P281 | При необходимости используйте средства индивидуальной защиты. |
| P282 | Наденьте защитные перчатки/лицевой щиток/защитные очки для защиты от холода. |
| P283 | Носите огнестойкую/огнестойкую/не распространяющую горение одежду. |
| P284 | Носите средства защиты органов дыхания. |
| P285 | В случае недостаточной вентиляции используйте средства защиты органов дыхания. |
| Р231 + Р232 | Работайте в среде инертного газа.Беречь от влаги. |
| Р235 + Р410 | Сохранять хладнокровие.Беречь от солнечных лучей. |
Ответ
| Код | Фраза |
| P301 | ПРИ ПРОГЛАТЫВАНИИ: |
| P304 | ПРИ ВДЫХАНИИ: |
| P305 | ПРИ ПОПАДАНИИ В ГЛАЗА: |
| P306 | ЕСЛИ НА ОДЕЖДЕ: |
| P307 | ЕСЛИ подвергается воздействию: |
| P308 | ЕСЛИ подверглись воздействию или обеспокоены: |
| P309 | ЕСЛИ подверглись воздействию или если вы плохо себя чувствуете: |
| P310 | Немедленно позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| P311 | Позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| P312 | Если вы плохо себя чувствуете, позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| P313 | Получите медицинскую консультацию/помощь. |
| P314 | Получите медицинскую консультацию/помощь, если вы плохо себя чувствуете. |
| P315 | Получите немедленную медицинскую консультацию/помощь. |
| Р320 | |
| Р302 + Р352 | ПРИ ПОПАДАНИИ НА КОЖУ: промыть большим количеством воды с мылом. |
| P321 | |
| P322 | |
| Р330 | Прополоскать рот. |
| P331 | Не вызывает рвоту. |
| P332 | ПРИ раздражении КОЖИ: |
| P333 | Если возникает раздражение кожи или сыпь: |
| P334 | Погрузить в прохладную воду/обернуть влажными бинтами. |
| P335 | Стряхните с кожи свободные частицы. |
| P336 | Оттаивайте обмороженные части теплой водой.Не трите пораженный участок. |
| P337 | Если раздражение глаз не проходит: |
| P338 | Снимите контактные линзы, если они есть и это легко сделать.Продолжайте полоскать. |
| Р340 | Вынести пострадавшего на свежий воздух и обеспечить ему покой в удобном для дыхания положении. |
| P341 | При затруднении дыхания вывести пострадавшего на свежий воздух и обеспечить ему покой в удобном для дыхания положении. |
| P342 | При появлении респираторных симптомов: |
| Р350 | Аккуратно промойте большим количеством воды с мылом. |
| P351 | Осторожно промойте водой в течение нескольких минут. |
| P352 | Вымойте большим количеством воды с мылом. |
| P353 | Промойте кожу водой/душем. |
| P360 | Немедленно промойте загрязненную одежду и кожу большим количеством воды, прежде чем снимать одежду. |
| P361 | Немедленно снять/снять всю загрязненную одежду. |
| P362 | Снять загрязненную одежду и постирать ее перед повторным использованием. |
| P363 | Постирайте загрязненную одежду перед повторным использованием. |
| Р370 | В случае пожара: |
| P371 | В случае крупного пожара и больших количеств: |
| P372 | Опасность взрыва в случае пожара. |
| P373 | НЕ тушите огонь, когда огонь достигает взрывчатых веществ. |
| P374 | Тушить огонь с разумного расстояния, соблюдая обычные меры предосторожности. |
| P376 | Остановите утечку, если это безопасно.Окисляющие газы (раздел 2.4) 1 |
| P377 | Пожар с утечкой газа: Не тушите, если утечку нельзя остановить безопасным образом. |
| P378 | |
| P380 | Эвакуация района. |
| P381 | Устраните все источники воспламенения, если это безопасно. |
| P390 | Поглотите пролитое вещество, чтобы предотвратить материальный ущерб. |
| P391 | Собрать разлив.Опасен для водной среды |
| Р301 + Р310 | ПРИ ПРОГЛАТЫВАНИИ: Немедленно обратиться в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| Р301 + Р312 | ПРИ ПРОГЛАТЫВАНИИ: ЕСЛИ вы плохо себя чувствуете, позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/врачу. |
| Р301 + Р330 + Р331 | ПРИ ПРОГЛАТЫВАНИИ: Прополоскать рот.Не вызывает рвоту. |
| Р302 + Р334 | ПРИ ПОПАДАНИИ НА КОЖУ: погрузить в прохладную воду/завернуть влажными бинтами. |
| Р302 + Р350 | ПРИ ПОПАДАНИИ НА КОЖУ: Аккуратно промойте большим количеством воды с мылом. |
| Р303 + Р361 + Р353 | ПРИ ПОПАДАНИИ НА КОЖУ (или волосы): Немедленно снять всю загрязненную одежду.Промойте КОЖУ водой/душем. |
| Р304 + Р312 | ПРИ ВДЫХАНИИ: При плохом самочувствии позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| Р304 + Р340 | ПРИ ВДЫХАНИИ: Вынести пострадавшего на свежий воздух и обеспечить ему покой в удобном для дыхания положении. |
| Р304 + Р341 | ПРИ ВДЫХАНИИ: Если дыхание затруднено, вынесите пострадавшего на свежий воздух и дайте ему отдохнуть в удобном для дыхания положении. |
| Р305 + Р351 + Р338 | ПРИ ПОПАДАНИИ В ГЛАЗА: осторожно промывать водой в течение нескольких минут.Снимите контактные линзы, если они есть и это легко сделать.Продолжайте полоскать. |
| Р306 + Р360 | ПРИ ПОПАДАНИИ НА ОДЕЖДУ: Немедленно промыть загрязненную ОДЕЖДУ и КОЖУ большим количеством воды, прежде чем снимать одежду. |
| Р307 + Р311 | ПРИ воздействии: обратиться в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| Р308 + Р313 | ПРИ воздействии или обеспокоенности: обратитесь за медицинской консультацией/помощью. |
| Р309 + Р311 | ПРИ воздействии или при плохом самочувствии: позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| Р332 + Р313 | ПРИ раздражении КОЖИ: обратиться к врачу. |
| Р333 + Р313 | ПРИ РАЗДРАЖЕНИИ КОЖИ или сыпи: обратиться к врачу. |
| Р335 + Р334 | Стряхните с кожи свободные частицы.Погрузить в прохладную воду/завернуть влажными бинтами. |
| Р337 + Р313 | ЕСЛИ раздражение глаз не проходит: обратиться к врачу. |
| Р342 + Р311 | ПРИ появлении респираторных симптомов: позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/терапевту. |
| Р370 + Р376 | В случае пожара: Остановите утечку, если это безопасно. |
| Р370 + Р378 | В случае пожара: |
| Р370 + Р380 | В случае пожара: Покиньте зону. |
| Р370 + Р380 + Р375 | В случае пожара: Покиньте зону.Тушить пожар дистанционно из-за риска взрыва. |
| Р371 + Р380 + Р375 | В случае крупного пожара и больших количеств: Покиньте зону.Тушить пожар дистанционно из-за риска взрыва. |
Хранилище
| Код | Фраза |
| P401 | |
| P402 | Хранить в сухом месте. |
| P403 | Хранить в хорошо проветриваемом месте. |
| P404 | Хранить в закрытой таре. |
| P405 | Хранить под замком. |
| P406 | Хранить в коррозионностойком/коррозионностойком контейнере с устойчивым внутренним вкладышем. |
| P407 | Обеспечьте воздушный зазор между штабелями/поддонами. |
| P410 | Беречь от солнечных лучей. |
| P411 | |
| P412 | Не подвергайте воздействию температур выше 50 oC/122 oF. |
| P413 | |
| Р420 | Хранить отдельно от других материалов. |
| P422 | |
| Р402 + Р404 | Хранить в сухом месте.Хранить в закрытой таре. |
| Р403 + Р233 | Хранить в хорошо проветриваемом месте.Держите контейнер плотно закрытым. |
| Р403 + Р235 | Хранить в хорошо проветриваемом месте.Сохранять хладнокровие. |
| Р410 + Р403 | Беречь от солнечных лучей.Хранить в хорошо проветриваемом месте. |
| Р410 + Р412 | Беречь от солнечных лучей.Не подвергайте воздействию температур выше 50°C/122°F. |
| Р411 + Р235 | Сохранять хладнокровие. |
Утилизация
| Код | Фраза |
| P501 | Утилизируйте содержимое/контейнер в... |
| P502 | Обратитесь к производителю/поставщику за информацией о восстановлении/переработке. |
Физические опасности
| Код | Фраза |
| H200 | Нестабильное взрывчатое вещество |
| Н201 | Взрывной;опасность взрыва массой |
| Н202 | Взрывной;серьезная опасность разбрасывания |
| Н203 | Взрывной;опасность пожара, взрыва или разбрасывания |
| Н204 | Опасность возгорания или разбрасывания |
| Н205 | Может масса взорваться в огне |
| H220 | Чрезвычайно легковоспламеняющийся газ |
| H221 | Горючий газ |
| H222 | Чрезвычайно легковоспламеняющийся аэрозоль |
| H223 | Легковоспламеняющийся аэрозоль |
| H224 | Чрезвычайно легковоспламеняющаяся жидкость и пар |
| H225 | Легковоспламеняющаяся жидкость и пар |
| H226 | Легковоспламеняющаяся жидкость и пар |
| H227 | Горючая жидкость |
| H228 | Легковоспламеняющееся твердое вещество |
| H229 | Контейнер под давлением: может лопнуть при нагревании |
| H230 | Может реагировать со взрывом даже в отсутствие воздуха |
| H231 | Может реагировать со взрывом даже в отсутствие воздуха при повышенном давлении и/или температуре |
| H240 | Нагрев может привести к взрыву |
| H241 | Нагрев может привести к пожару или взрыву |
| Н242 | Отопление может привести к пожару |
| H250 | Самопроизвольно воспламеняется при контакте с воздухом |
| H251 | Самонагрев;может загореться |
| H252 | Самонагрев в больших количествах;может загореться |
| H260 | При контакте с водой выделяет легковоспламеняющиеся газы, которые могут самовозгораться |
| H261 | При контакте с водой выделяет легковоспламеняющийся газ |
| H270 | Может вызвать или усилить пожар;окислитель |
| H271 | Может вызвать пожар или взрыв;сильный окислитель |
| H272 | Может усилить огонь;окислитель |
| H280 | Содержит газ под давлением;может взорваться при нагревании |
| H281 | Содержит охлажденный газ;может вызвать криогенные ожоги или травмы |
| H290 | Может вызывать коррозию металлов |
Опасности для здоровья
| Код | Фраза |
| Н300 | Смертельно при проглатывании |
| H301 | Токсично при проглатывании |
| H302 | Вред при проглатывании |
| H303 | Может быть вреден при проглатывании |
| H304 | Может быть смертельным при проглатывании и попадании в дыхательные пути |
| H305 | Может быть вредным при проглатывании и попадании в дыхательные пути |
| H310 | Смертельно при контакте с кожей |
| H311 | Токсичен при контакте с кожей |
| H312 | Вреден при контакте с кожей |
| H313 | Может быть вредным при попадании на кожу |
| H314 | Вызывает сильные ожоги кожи и повреждение глаз |
| H315 | Вызывает раздражение кожи |
| H316 | Вызывает легкое раздражение кожи |
| H317 | Может вызвать аллергическую реакцию кожи |
| H318 | Вызывает серьезные повреждения глаз |
| H319 | Вызывает серьезное раздражение глаз |
| H320 | Вызывает раздражение глаз |
| H330 | Смертельно при вдыхании |
| H331 | Токсичен при вдыхании |
| H332 | Вреден при вдыхании |
| H333 | Может быть вредным при вдыхании |
| H334 | При вдыхании может вызвать симптомы аллергии или астмы или затрудненное дыхание |
| H335 | Может вызывать раздражение дыхательных путей |
| H336 | Может вызвать сонливость или головокружение |
| H340 | Может вызывать генетические дефекты |
| H341 | Подозревается в возникновении генетических дефектов |
| H350 | Может вызвать рак |
| H351 | Подозревается в развитии рака |
| H360 | Может повредить фертильность или нерожденному ребенку |
| H361 | Подозревается в нарушении фертильности или нерожденного ребенка |
| H361d | Подозревается в причинении вреда будущему ребенку |
| H362 | Может причинить вред детям, находящимся на грудном вскармливании |
| H370 | Вызывает поражение органов |
| H371 | Может привести к повреждению органов |
| H372 | Вызывает повреждение органов при длительном или многократном воздействии |
| H373 | Может вызывать повреждение органов при длительном или многократном воздействии |
Опасности для окружающей среды
| Код | Фраза |
| H400 | Очень токсичен для водных организмов |
| H401 | Токсичен для водных организмов |
| H402 | Вреден для водных обитателей |
| H410 | Очень токсичен для водных организмов с долгосрочными последствиями |
| H411 | Токсично для водных организмов с долгосрочными последствиями |
| H412 | Вреден для водных организмов с долгосрочными последствиями |
| H413 | Может вызывать долгосрочные вредные последствия для водных организмов |
| H420 | Наносит вред здоровью населения и окружающей среде, разрушая озон в верхних слоях атмосферы. |
Применение в синтезе [ 5402-55-1 ]
Восходящий маршрут синтеза [ 5402-55-1 ]
Синтетический маршрут вниз по течению [ 5402-55-1 ]
Восходящий маршрут синтеза [ 5402-55-1 ]
| Урожай | Условия реакции | Эксплуатация в эксперименте |
|---|---|---|
| 72% | Со штаммом зигомицета S.racemosum MUT 770 В диметилсульфоксиде в течение 72 ч;Ферментативная реакция | 2.3.Эксперименты по биотрансформации. Штаммы грибов предварительно выращивали в чашках Петри, содержащих твердую среду maltextract (МЭА: 20 г л-1 глюкозы, 20 г л-1 солодового экстракта, 20 г л-1 агара, 2 г л-1 пептона), из которых инокулят для жидких культур.Грибок инокулировали в виде суспензии конидий (1·106 конидий/мл) в 50 мл колб, содержащих 40 мл жидкой среды maltextract.Колбы инкубировали при 25°С и поддерживали при перемешивании (110 об/мин). Через 2 дня предварительного выращивания добавляли 500 мМ раствор субстрата в ДМСО до исходной концентрации субстрата (с0) 1–5 мМ.Для каждого субстрата проводили три биологические повторности. Эксперимент проводили в течение 3 дней после добавления субстратов, в течение которых отбирали образцы объемом 1 мл через определенные промежутки времени (обычно 24, 48 и 72 ч).Каждый образец экстрагировали EtOAc (500 л), органическую фазу сушили над безводным Na2SO4 и анализировали с помощью ГХ/МС.В некоторых случаях (см. раздел 2.4) было проведено выделение восстановленного продукта. Для каждого набора биотрансформаций использовали один опрос для измерения исходной биомассы и рН перед добавлением субстрата. Эти параметры также были оценивается в конце эксперимента по всем вопросам.Жидкую среду отделяли от биомассы путем фильтрации и использовали для измерения рН, в то время как мицелий сушили при 60°С в течение 24 часов для измерения сухой массы биомассы.2-(тиофен-2-ил)этанол: из 2-(тиофен-2-ил)уксусной кислоты (3,7 мг, 72%) и из метил-2-(тиофен-2-ил)ацетата (24,6 мг, 96%).1H ЯМР (400 МГц, CDCl3, ТМС): = 7,20 (м, 1H, гетероароматический водород), 6,99 (м, 1H, гетероароматический водород), 6,90 (м, 1H, гетероароматический водород), 3,85 (т, 2H, J = 6,2 Гц, CH2OH), 3,02 (т, 2H, J = 6,2 Гц, CH2CH2OH).13С ЯМР (100 МГц, CDCl3, ТМС): = 140,5, 127,0, 125,8, 124,0, 63,4, 33,3.ГХ/МС: tR = 9,47 мин, m/z128 (М+, 30), 110 (5), 97 (100) |
| 66,5% | Стадия № 1: с тетрагидридом лития-алюминия в тетрагидрофуране при 0–20 ℃; Этап №2: С водой;хлорид натрия в тетрагидрофуране при 0℃; | Шаг 9 2-(тиофен-2-ил)этанол: При температуре около 0°C к суспензии алюмогидрида лития (0,534 г; 14,05 ммоль) в сухом тетрагидрофуран (10 мл). Смесь перемешивали при температуре окружающей среды в течение примерно 4 часов, а затем охлаждали примерно до 0°С. После добавления холодного насыщенного раствора хлорида натрия (1 мл) смесь фильтровали и неорганические соли промывали тетрагидрофураном и этилацетатом. Фильтрат и промывные воды объединяли и концентрировали в вакууме с получением указанного в заголовке соединения в виде коричневого масла (0,600 г, 66,5%). 1H ЯМР (400 МГц, CDCl3) δ 1,60 (ш., заменяемый на D2O, 1H), 3,08 (т, J=6,2 Гц, 2H), 3,85 (т, J=6,2 Гц, 2H), 6,87-6,88 (м, 1H), 6,95-6,97 (м, 1H), 7,16-7,25 (м, 1ч).ИК (пленка) υ 3345, 3105, 2211, 2126, 2090, 1792, 1433, 1138, 972, 737, 699 см-1МС: 129 (М+1). |
| Урожай | Условия реакции | Эксплуатация в эксперименте |
|---|---|---|
| 96% | Со штаммом зигомицета S.racemosum MUT 770 В диметилсульфоксиде в течение 72 ч;Ферментативная реакция | 2.3.Эксперименты по биотрансформации. Штаммы грибов предварительно выращивали в чашках Петри, содержащих твердую среду maltextract (МЭА: 20 г л-1 глюкозы, 20 г л-1 солодового экстракта, 20 г л-1 агара, 2 г л-1 пептона), из которых инокулят для жидких культур.Грибок инокулировали в виде суспензии конидий (1·106 конидий/мл) в 50 мл колб, содержащих 40 мл жидкой среды maltextract.Колбы инкубировали при 25°С и поддерживали при перемешивании (110 об/мин). Через 2 дня предварительного выращивания добавляли 500 мМ раствор субстрата в ДМСО до исходной концентрации субстрата (с0) 1–5 мМ.Для каждого субстрата проводили три биологические повторности. Эксперимент проводили в течение 3 дней после добавления субстратов, в течение которых отбирали образцы объемом 1 мл через определенные промежутки времени (обычно 24, 48 и 72 ч).Каждый образец экстрагировали EtOAc (500 л), органическую фазу сушили над безводным Na2SO4 и анализировали с помощью ГХ/МС.В некоторых случаях (см. раздел 2.4) было проведено выделение восстановленного продукта. Для каждого набора биотрансформаций использовали один опрос для измерения исходной биомассы и рН перед добавлением субстрата. Эти параметры также были оценивается в конце эксперимента по всем вопросам.Жидкую среду отделяли от биомассы путем фильтрации и использовали для измерения рН, в то время как мицелий сушили при 60°С в течение 24 часов для измерения сухой массы биомассы.2-(тиофен-2-ил)этанол: из 2-(тиофен-2-ил)уксусной кислоты (3,7 мг, 72%) и из метил-2-(тиофен-2-ил)ацетата (24,6 мг, 96%).1H ЯМР (400 МГц, CDCl3, ТМС): = 7,20 (м, 1H, гетероароматический водород), 6,99 (м, 1H, гетероароматический водород), 6,90 (м, 1H, гетероароматический водород), 3,85 (т, 2H, J = 6,2 Гц, CH2OH), 3,02 (т, 2H, J = 6,2 Гц, CH2CH2OH).13С ЯМР (100 МГц, CDCl3, ТМС): = 140,5, 127,0, 125,8, 124,0, 63,4, 33,3.ГХ/МС: tR = 9,47 мин, m/z128 (М+, 30), 110 (5), 97 (100) |
Синтетический маршрут вниз по течению [ 5402-55-1 ]
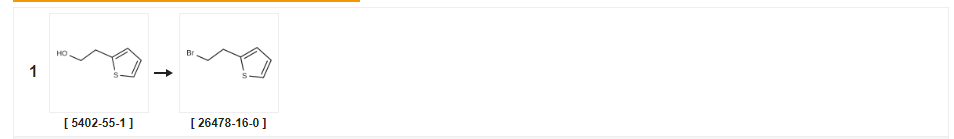
| Урожай | Условия реакции | Эксплуатация в эксперименте |
|---|---|---|
| 94% | с четырехбромистым углеродом;трифенилфосфин В тетрагидрофуране при 0℃;техника Шленка;Инертная атмосфера; | |
| 69% | с бромом;трифенилфосфин в дихлорметане при 20℃; | |
| 64% | P.31 Синтез 2-(2-бромэтил)тиофена Пример получения 31. Синтез 2-(2-бромэтил)тиофена. 2-Тиенилэтанол (0,44 мл) обрабатывали, как описано выше в примере получения 1, с получением указанного в заголовке соединения (0,490 г) в виде бесцветного масла (выход: 64,0%).1H-ЯМР (400 МГц, CDCl3): δ (м.д.) 3,38 (2H, т, J=7,6 Гц), 3,58 (2H, т, J=7,6 Гц), 6,89 (1H, д, J=1,2 Гц), 6,96 (1H, д, J=4,2 Гц), 7,19 (1H, дд, J=1,2, 4,2 Гц). |
| 28% | С трибромидом фосфора в дихлорметане при 0 - 20 ℃;на 1ч; | |
| 19% | С трибромидом фосфора в тетрахлорметане при 65 ℃;за 0,333333 ч; | a Трибромид фосфора (2,0 мл, 21,1 ммоль) добавляли к перемешиваемому раствору 2-(тиофен-2-ил)этанола (2,25 г, 17,6 ммоль) в четыреххлористом углероде (162 мл), затем смесь нагревали при 65°С в течение 20 минут.Смеси давали охладиться до температуры окружающей среды, затем добавляли лед.Органический слой отделяли, затем водный слой экстрагировали дихлорметаном (2×30 мл).Объединенные органические слои промывали рассолом, затем сушили (NaSO4), фильтровали и концентрировали в вакууме.Остаток очищали флэш-хроматографией на диоксиде кремния, элюируя смесями этилацетат:гексан от 0:100 до 0,5:95,5, с получением 2-(2-бромэтил)тиофена в виде коричневого масла (650 мг, 19%). |
| с пиридином;хлороформ;трибромид фосфора | ||
| С трибромидом фосфора в диэтиловом эфире при 0℃;на 4 часа; | 2D Пример 2D;9-(4,5-Диметил-тиазол-2-ил)-4-[4-(2-тиофен-2-ил-этил)-пиперазин-1-ил]-5,6,7,8-ТЕТРАГИДРО- 1, 3, 4B-ТРИАЗА-ФЛУОРЕН К раствору 2-(2-тиенил)этанола (1,63 г) в сухом эфире (15 мл) при 0°C по каплям добавляли PBr3 (1,31 мл).Через 4 часа реакционную смесь разбавляли дихлорметаном, промывали водой, сушили (MGS04) и растворитель удаляли в вакууме с получением коричневого масла, которое очищали с помощью флэш-хроматографии с получением 2-(2-бромэтил)тиофена.Смесь 9-(4,5-ДИМЕТИЛ-ТИАЗОЛ-2-ИЛ)-4-ПИПЕРАЗИН-1-ИЛ-5,6,7,8-ТЕТРАГИДРО-1,3,4b-триаза-флуорена (85мг), 2-(2-бромэтил)тиофен (44 мг) и карбонат калия (38 мг) нагревали с обратным холодильником в ацетонитриле (5 мл) в течение 4 часов.Реакционную смесь охлаждали, экстрагировали дихлорметаном, сушили (MGS04) и растворитель удаляли в вакууме с получением сырого продукта, который очищали с помощью флэш-хроматографии с получением указанного в заголовке соединения (30 мг). |
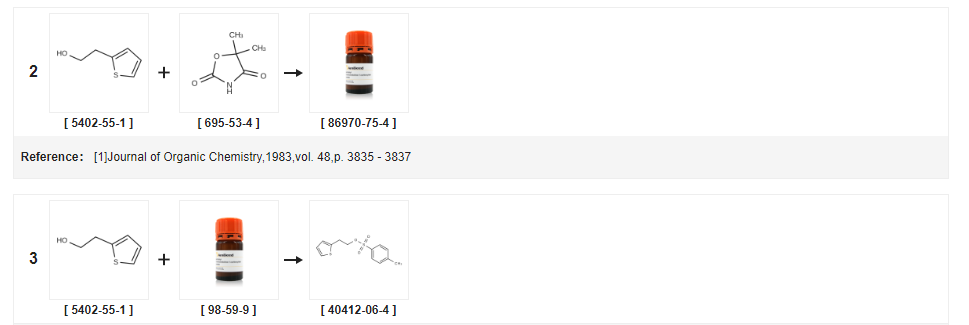
| Урожай | Условия реакции | Эксплуатация в эксперименте |
|---|---|---|
| 98% | с триэтиламином;при 35℃; Охлаждение льдом; | В трехгорлую колбу емкостью 1 л последовательно добавляли (0,87 моль) 2-тиофенэтанола и 184 г (0,97 моль) п-толуолсульфонилхлорида, туда по каплям добавляли 98 г (0,97 моль) триэтиламина на бане со льдом и водой, И поддерживают температуру реакционной жидкости не выше 20°С, заканчивают прикапывание, нагревают до 35°С, продолжают перемешивание, соответственно 24ч, 27ч отбор проб, ТСХ, до завершения реакции, останавливают реакцию, фильтруют, осадок на фильтре с соответствующими количество дихлорметана А. Слой хлористого метилена сушили безводным сульфатом натрия в течение 2 часов.Осушитель отфильтровывали и осушитель промывали небольшим количеством метиленхлорида.Фильтрат декомпрессировали в вакууме и фильтрат упаривали при пониженном давлении.Концентрированное до постоянного веса коричневое масло весом 203 г, выход 98%, |
| 96,37% | с триэтиламином;в толуоле;при 5 - 30℃;за 20,8333 ч; Распределение продукта / селективность; | ПРИМЕР 3 Получение 2-тиенилэтилпара-толуолсульфоната (формула VII) с использованием толуола. В чистый и сухой реактор загружали 400 литров толуола и 163,2 кг пара-толуолсульфонилхлорида с последующим охлаждением примерно до 5°С. 2-этанол добавляли примерно при 5°С в течение примерно 20 минут с последующим добавлением 130 кг триэтиламина в течение примерно 8 часов 50 минут.Температуру реакционной смеси повышают примерно до 30°С с последующим перемешиванием в течение примерно 12 часов.Реакционную массу фильтровали через нутч-фильтр и промывали 2×100 л толуола.Реакционный фильтрат переносили в другой реактор с последующей промывкой 5×200 л воды.Органический и водный слои разделяли и органический слой полностью перегоняли при температуре ниже 70°С в вакууме с получением 212 кг (выход: 96,37%) указанного в заголовке соединения.Чистота по ГХ: 95,59%. |
| 96,5% | с триэтиламином;В дихлорметане;при -5 - 20℃;на 2 часа; | 32,7 г (0,17 моль) п-толуолсульфонилхлорида, 40 мл дихлорметана в реакционную колбу, охлажденную до -5°С, 20 г (0,16 моль) 2-тиофенэтанола. Медленно по каплям добавляли 28,4 г (0,28 моль) триэтиламина и температуру реакционного раствора поддерживали около 0°С. Плюс Bi выдерживали в течение 2 ч после того, как реакционная смесь была нагрета до комнатной температуры.2-тиофеновый этанол израсходовали до получения сырья, фильтровали с отсасыванием. Твердое вещество промывали небольшим количеством метиленхлорида, фильтрат промывали 50 мл насыщенного бикарбоната натрия и сушили над безводным сульфатом натрия.Фильтрование, концентрирование фильтрата, выпадение в осадок светло-коричневого твердого вещества. Фильтрование, промывание небольшим количеством петролейного эфира до белого цвета. Это 42,5 г этилового эфира п-толуолсульфоната-2-тиофена, выход 96,5% (чистота по ВЭЖХ 99%). |
| 95,5% | с триэтиламином;В дихлорметане;при 7,5 - 22,5 ℃;за 5ч;Распределение продукта/избирательность; | ПРИМЕР 10. Получение тозилата 2-(2-тиофен)этанола (формула VII) с использованием дихлорметана. 4 литра дихлорметана добавляли в реактор при температуре около 30°С, охлаждали до температуры около 7,5°С и добавили 1,784 кг п-толуолсульфонилхлорида, а затем 1 кг тиофен-2-этанола.К вышеуказанной реакционной массе добавляли 1,302 кг триэтиламина при температуре примерно 7,5°С с последующим медленным повышением температуры реакционной массы до 22,5°С в течение примерно 5 часов.Полученную реакционную массу фильтровали через напорный нутч-фильтр, промывали хлористым метиленом (2×1 л), собирали маточный раствор и переносили в другой реактор.Органический слой промывали водой (5×2 литра).Полученный таким образом органический слой подвергали перегонке при температуре ниже 70°С с использованием циркуляции горячей воды.Затем полученный остаток охлаждали примерно до 30°С, получая 2,1 кг (выход: 95,5%) указанного в заголовке соединения. |
| 93,6% | с триэтиламином;в толуоле;при 45℃;на 4 часа; | Пример 1 0,2.Превращение гидробромида (S)-1,2,3,4-тетрагидро-5-гидрокси-N-пропилнафталин-2-аммония (VIII) в гидрохлорид ротиготина;10.2.1.Получение 2-(2-тиенил)этил-4-толуолсульфоната;Объединяют 4-толуолсульфонилхлорид (162 г), толуол (363,3 г) и 2-(2-тиенил)этанол (104 г).Добавляют триэтиламин (93 г), поддерживая температуру ниже 45°С. Через 4 часа смесь промывают водным раствором фосфорной кислоты, водным раствором гидроксида натрия и затем водой.Органическую фазу отгоняют в вакууме.Добавляют изопропанол (314 г) и гептаны (365,9 г).Партию кристаллизуют при охлаждении и выделяют при -15°С. Кристаллы фильтруют и промывают гептанами (175 мл).Затем кристаллы сушат в вакууме при комнатной температуре до достижения точки плавления > 30°С. Выход (214 г): 93,6 % Анализы ВЭЖХ подтвердили чистоту > 99 % и 100 % анализ по сравнению с эталонным стандартом. |
| 93,6% | с триэтиламином;в толуоле;при 45℃;на 4 часа; | Объединяют 4-толуолсульфонилхлорид (162 г), толуол (363,3 г) и 2-(2-тиенил)этанол (104 г).Добавляют триэтиламин (93 г), поддерживая температуру ниже 45°С. Через 4 часа смесь промывают водным раствором фосфорной кислоты, водным раствором гидроксида натрия и затем водой.Органическую фазу отгоняют в вакууме.Добавляют изопропанол (314 г) и гептаны (365,9 г).Партию кристаллизуют при охлаждении и выделяют при -15°С. Кристаллы фильтруют и промывают гептанами (175 мл).Затем кристаллы сушат в вакууме при комнатной температуре до достижения температуры плавления 30°С.[0255] Выход (214 г): 93,6%. |
| 90% | с силикагелем;В дихлорметане;на 2ч;Рефлюкс; | 12,8 г (0,1 моль) 2-(2-тиенил)этанола, 1000 мл дихлорметана, 21,0 г (0,12 моль) хлорангидрида п-толуолсульфоновой кислоты и 10,0 г силикагеля в реакционную колбу, реакционную смесь кипятили с обратным холодильником в течение 2 часов, охлаждали, фильтровали для удаления силикагеля. Реакционную смесь последовательно промывали дистиллированной водой, насыщенным раствором карбоната натрия, рассолом, затем растворитель метиленхлорид удаляли перегонкой при пониженном давлении, получая 26,0 г п-толуолсульфокислоты. Получение 2 - (2-тиенил)этиловый эфир, выход 90%. |
| В пиридине;вода; | (а) Тозилат 2-(2-гидроксиэтил)тиофена Толуол-4-сульфонилхлорид (4,125 г) порциями добавляли в течение 5 минут к охлажденному льдом раствору 2-(2-гидроксиэтил)тиофена (1,723 г) в безводном пиридине. (20 мл) и полученный бледно-желтый раствор перемешивали при 0°С. Через 3 часа реакционную смесь выливали в энергично перемешиваемую воду (160 мл), получая осадок.После охлаждения твердое вещество собирали и промывали водой с получением белых кристаллов указанного в заголовке тозилата (3,555 г), т.пл. 33-34°С, лямбдамакс (EtOH) 227 нм (Е11 612). | |
| с триэтиламином;В бутаноне;при 0 - 30 ℃; | Пример 1 Получение 2-(2-тиенил)этилпара-толуолсульфоната. Смесь п-толуолсульфонилхлорида (328 г) и 2-(2-тиенил)этанола (200 г) в метилэтилкетоне (1000 мл) готовили. охлаждается до 0С.После этого добавляли по каплям триэтиламин (283,1 мл) при 0-5°С в течение 1-2 часов и реакционную массу перемешивали в течение 12-15 часов при 25-30°С.Полученную массу фильтровали и промывали метилэтилкетоном (500 мл).Полученный органический слой промывали водой (500 мл) с последующим промыванием насыщенным раствором бикарбоната натрия (500 мл) и раствором соли (500 мл).Полученный органический слой перегоняли в вакууме при температуре ниже 50°С с получением 2-(2-тиенил)этилпара-толуолсульфоната в виде маслянистой массы (масса масла: 505 г; чистота по данным ВЭЖХ: 97%). | |
| с триэтиламином;В бутаноне;при 0 - 30 ℃; | Пример 1 Получение 2-(2-тиенил)этилпара-толуолсульфоната. Смесь п-толуолсульфонилхлорида (328 г) и 2-(2-тиенил)этанола (200 г) в метилэтилкетоне (1000 мл) готовили. охлаждали до 0°С. После этого добавляли по каплям триэтиламин (283,1 мл) при 0-5°С в течение 1-2 часов, и реакционную массу перемешивали в течение 12-15 часов при 25-30°С. Полученную массу фильтровали и промывали метилэтилкетоном (500 мл).Полученный органический слой промывали водой (500 мл) с последующим промыванием насыщенным раствором бикарбоната натрия (500 мл) и раствором соли (500 мл).Полученный органический слой перегоняли в вакууме при температуре ниже 50°С, получая 2-(2-тиенил)этилпара-толуолсульфонат в виде маслянистой массы (масса масла: 505 г; чистота по ВЭЖХ: 97%). | |
| с карбонатом калия;в толуоле;при 0 - 20 ℃;на 3,5 часа; | В реакционную колбу на 1000 мл добавляли 500 мл толуола, 50 г тиофенового этанола и 80 г п-толуолсульфонилхлорида, включали перемешивание, при контролируемой температуре добавляли по каплям при 0°С 64 г карбоната калия. закончили нагревание реакции до 20°С в течение 3 часов. К реакционному раствору добавили 400 мл воды. Дважды промыли. Промытый толуольный слой непосредственно использовали для следующей реакции. | |
| с N-этил-N,N-диизопропиламином;в толуоле;при 0 - 20 ℃;на 3,5 часа; | В реакционную колбу на 1000 мл добавляли 500 мл толуола, 50 г тиофенового этанола и 92 г п-толуолсульфонилхлорида, перемешивали при 0°С, по каплям добавляли 62 г N,N-диизопропилэтиламина в течение примерно 30 мин.По завершении прикапывания смесь нагревали до 20°С и реагировали в течение 3 часов.К реакционному раствору добавляли 400 мл воды, дважды промывали, промытый толуольный слой непосредственно использовали для следующей реакции. | |
| с триэтиламином;в толуоле;при 0 - 20 ℃;на 3 часа; | 500 мл толуола, 50 г тиофенового этанола и 80 г п-толуолсульфонилхлорида помещали в реакционную колбу на 1000 мл и повышали температуру до 20°С в течение 3 часов.К реакционному раствору добавляли 400 мл воды, дважды промывали, промывали толуолом, наслаивали непосредственно на следующую стадию реакции. | |
| с карбонатом калия;в толуоле;при 0 - 20 ℃;на 3,5 часа; | В реакционную колбу вместимостью 1000 мл помещали 500 мл толуола, 50 г тиофенового этанола и 107 г п-толуолсульфонилхлорида, включали перемешивание, поддерживали температуру на уровне 0°С, добавляли по каплям 64 г карбоната калия, добавление длилось около 30 мин, после чего нагревали до 20°С и реагировали в течение 3 ч, к реакционному раствору добавляли 400 мл воды, дважды промывали, и промытый толуольный слой непосредственно использовали для следующей реакции. | |
| с триэтиламином;в толуоле;при 0 - 25 ℃;на 3,5 часа; | Пример 1. Способ получения гидрохлорида тиклопидина, показанный на фиг. 2, включает следующие стадии: 1.п-толуолсульфонилзащита: В реакционную колбу на 1000 мл загружали 500 мл толуола, 50 г тиофенового этанола и 80 г п-толуолсульфонилхлорида и перемешивали для контроля. При температуре 0°С по каплям добавляли 47 г триэтиламина, капали в течение примерно 30 мин, и температуру повышали до 25°С в течение 3 часов. Добавляли 400 мл воды, дважды промывали, промывали слой толуолом непосредственно к следующей стадии реакции.2.Реакция конденсации Реакционный раствор толуола на предыдущей стадии добавляли в реакционную колбу на 1000 мл с последующим добавлением 114 г о-хлорбензиламина и нагреванием до 90°С в течение 3 часов.После реакции смесь охлаждали до 25°С и перемешивали в течение 1 часа.К фильтрату добавляли 200 мл воды и соляной кислоты. Доводили рН системы до 8,5, расслаивали верхний слой толуола и продолжали по каплям соляной кислоты доводить рН до 5, затем охлаждали систему до 2 С. Кристаллы перемешивали в течение 4 ч, фильтруют и осадок на фильтре сушат в вакууме при 50°С, получая 96 г гидрохлорида конденсата.Реакция с замкнутым контуром. В реакционную колбу на 1000 мл добавляли 96 г гидрохлорида конденсата, 400 мл 1,3-диоксана и 5 мл соляной кислоты при 90°С в течение 6 часов.После реакции смесь охлаждали до 7°С и перемешивали в течение 3 часов.Осадок на фильтре промывали небольшим количеством 1,3-диоксетана. После сушки в вакууме при 50°С получали 95 г гидрохлорида тиклопидина 4 ?В реакционную колбу на 1000 мл добавляли 95 г неочищенного гидрохлорида тиклопидина и 500 мл абсолютного этанола и нагревали до 72°С при перемешивании. горячий фильтр, фильтрат постепенно охлаждается. Кристаллы кристаллизуют при 4°С в течение 4 часов и фильтруют.Осадок на фильтре промывают небольшим количеством абсолютного этанола и сушат в вакууме при 50°С, получая 91 г продуктов Precision гидрохлорида титиола.Общий выход 82%, чистота 99,9%. | |
| с гидроксидом натрия;В воде;толуол;при 10 - 55℃;на 11ч; | В трехгорлую колбу помещают 97 г п-толуолсульфонилхлорида и 180 мл толуола. Перемешивают и растворяют, фильтруют, поддерживают в тепле при 15-20°С, в трехгорлую колбу. 120 г 40% водного раствора гидроксида натрия, перемешивание. По каплям при 10-20°С добавляли раствор 97 г п-толуолсульфонилхлорида, растворенного в 180 мл толуола, и смесь перемешивали в течение 3 ч, затем нагревают до 45-55°С в течение 8 ч и оставляют для расслоения. Органическую фазу сбрасывают для удаления толуола с получением п-толуолсульфоната 2-(2-тиофен)этанола. Красновато-коричневое масло;молекулярная формула выглядит следующим образом: | |
| 235,1 г | с гидроксидом натрия;В хлороформе;при 0 - 5℃;на 12ч; | В реакционную колбу добавляют вышеуказанный этап 2-тиофеновый этанол: 112 г, хлороформ 600 г, PTSC 249,4 г, и смесь охлаждают до 0-5°C. Добавляют 834 г 10% по массе раствора гидроксида натрия, контролируя температуру 0 -5°С, выдерживают в тепле в течение 12 часов, добавляют соляную кислоту до pH=12, слой, водный слой экстрагируют 300 г хлороформа и объединяют слой хлороформа.После промывки 100 г воды органический слой перегоняли досуха, получая п-толуолсульфонат 2-тиофенэтанола: 235,1 г, выход 95,3%, чистота 99,5%. |
Напишите свое сообщение здесь и отправьте его нам

![[ CAS № 5402-55-1 ] 2-тиофенэтанол Рекомендуемое изображение](https://www.ohlsenwin.com/uploads/p1.png)
![[CAS № 5402-55-1] 2-тиофенэтанол](https://www.ohlsenwin.com/uploads/p1-300x300.png)
![[CAS № 5402-55-1] 2-тиофенэтанол](https://www.ohlsenwin.com/uploads/product-2-300x300.png)
![[CAS № 5402-55-1] 2-тиофенэтанол](https://www.ohlsenwin.com/uploads/product-1-300x300.png)




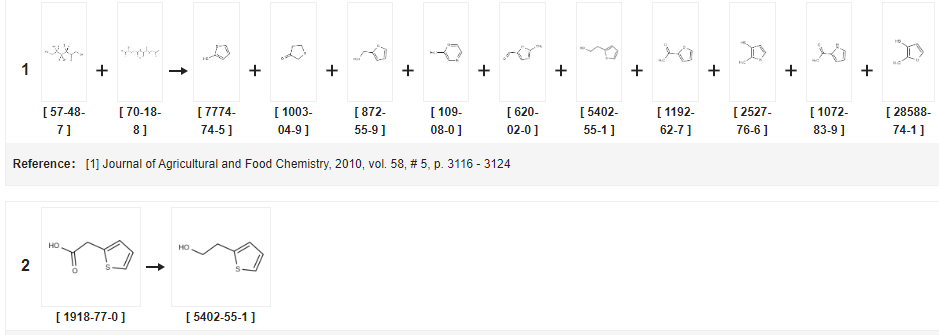

![[CAS № 141109-14-0] (S)-метил 2-амино-2-(2-хлорфенил)ацетат](https://www.ohlsenwin.com/uploads/Chlorophenylglycine-methyl-ester-2-300x300.png)
![[ CAS № 141109-19-5 ] (S)-метил 2-(2-хлорфенил)-2-((2-(тиофен-2-ил)этил)амино)ацетат гидрохлорид](https://www.ohlsenwin.com/uploads/Chlorophenylglycine-methyl-ester-31-300x300.png)
![[ CAS № 40412-06-4 ] 2-(тиофен-2-ил)этил 4-метилбензолсульфонат](https://www.ohlsenwin.com/uploads/ethanol-Tosylate-4-300x300.png)